ARCH ARGENT OFTALMOL | 2018
ARTÍCULO DE INTERÉS
Ojo seco: de dónde venimos, dónde estamos,
a dónde vamos
Relator:
Dr. Alejandro J. Aguilar
Co-Relator:
Dr. Alejandro Berra
INTRODUCCIÓN
El ojo seco ocupa un lugar de relevancia en la práctica oftalmológica diaria, así como también en las diferentes líneas de investigación que se desarrollan de manera cada vez más intensamente en esta habitual patología.
Es un hecho que un altísimo porcentaje de los pacientes que acuden a la consulta presentan signos y síntomas de esta enfermedad, y muchos de ellos la desarrollan.
Nuestro entendimiento sobre el ojo seco ha mejorado y aumentado considerablemente en los últimos años, lo que consecuentemente produjo un notorio y favorable cambio en los métodos diagnósticos y en la calidad de los tratamientos dirigidos a este particular desorden que compromete a la superficie ocular.
Este relato anual se propone brindar una referencia actualizada del síndrome de ojo seco, teniendo en cuenta el desarrollo evolutivo que ha tenido; desde sus primeras descripciones hasta la actualidad.
RESEÑA HISTÓRICA
La primera referencia a la que podemos acceder se encuentra en el papiro de Ebers 1, donde en el año 1500 a.C. se describe un fenómeno que afecta los ojos bajo el nombre de “xerosis”. Es Hipócrates 400 años a. C. quién describe dos cuadros clínicos en referencia a las lágrimas; uno por exceso y el otro por falta, a los que denominó certeramente “oftalmía húmeda” y “oftalmía seca” respectivamente.
En la época galo-romana, J. Voinot 2 recomienda un honorario para el manejo de pacientes con ojo seco y en el año 1808 M. de Wenzel 3, en su “Manuel del´Oculiste” hace un amplio relato de la enfermedad. Como dato curioso, este libro puede comprarse a través de la cadena internacional Amazon.
Siguiendo la descripción de Wenzel; W. Mackenzie 4 establece en 1856 un concepto clave que perdurará en el tiempo alcanzando nuestros días y que no sólo forma parte fundamental de la fisiopatología de la enfermedad, sino que también involucra a uno de los test de diagnóstico y numerosas líneas de tratamiento: “La xeroftalmía obedece a deficiencias del moco conjuntival”.
Ya en el siglo XX, específicamente en 1903, Otto Schirmer 5 describe los lineamientos del test que lleva su nombre y que nos acompaña hasta nuestros días.
En los años 20, y gracias a los trabajos de M. Gourgerot 6 comienza a darse forma a un síndrome que ocupó el interés de numerosos autores. Gourgerot en 1903 describe un proceso de insuficiencia progresiva y atrófica de las glándulas salivales que involucran a la mucosa bucal y conjuntival.
Este trabajo sirvió de base para que en 1933, y en colaboración con Gourgerot, Henry Sjögren 7 describiera a la queratoconjuntivitis sicca. Desde ese entonces, la queratoconjuntivitis sicca dominó la escena que he denominado: la primera ola.
LA PRIMERA OLA
Las descripciones del síndrome de Gourgerot-Sjögren fueron el puntapié inicial para que durante décadas se estimularan y dispararan trabajos y líneas de investigación sobre la queratoconjuntivitis sicca.
Esto determinó lo que he denominado “la primera ola”, fenómeno en particular que vinculaba a prácticamente todos los casos de ojo seco con la queratoconjuntivitis sicca, y un alto porcentaje de estos pacientes eran asociados al Síndrome de Sjögren.
Durante este particular período se desarrollaron los principales y fundamentales conceptos sobre la fisiopatología del ojo seco, su cascada de eventos, los métodos diagnósticos y las modalidades terapéuticas que hoy siguen vigentes. Desde este punto de vista, la primera ola resulta incomparable con la segunda ola, donde si bien surgen nuevos equipos dirigidos al diagnóstico y tratamiento de la disfunción de glándula de Meibomio, no hubo ni hay en esta segunda etapa conceptos clave ni superadores como los hubo durante la primera ola.
La intensidad y la fuerza de esta tendencia determinó que en 1952, Balik J. 8 describiera al fluido lagrimal en relación a la queratoconjuntivitis sicca. Botelho S., en 1964, estableció similares conceptos en su artículo sobre las lágrimas y las glándulas lagrimales, en clara alusión a las implicancias que el síndrome de Sjögren tenía sobre las mismas. Un año despúes y en forma prácticamente simultánea Mishima S. 9 y Ehlers N. 10 describen los principales aspectos del film pre-corneal respectivamente (Fig. 1).

Figura 1: El film lagrimal
Hasta ese entonces, el diagnóstico de ojo seco se basaba fundamentalmente en los resultados obtenidos al realizar el test de Schirmer y la tinción que se evidenciaba con el rosa de bengala.
Ese mismo año Brown S. I. 11 en colaboración con Mishima S., afianzan los aspectos fisiológicos del film lagrimal, hacen foco en el efecto del parpadeo sobre la concentración de la película lagrimal y marcan el camino hacia el tiempo de ruptura lagrimal, o break up time (BUT).
Todos estos autores afianzaron la composición estructural del film lagrimal con la presencia de sus tres capas: la superficial lipídica, la media acuosa y la interna mucosa.
Tomando como punto de partida el trabajo de Brown y Mishima anteriormente mencionado, Norm M. S. 12, en 1969, establece las bases definitivas del BUT, siendo su trabajo el que da forma final al tiempo de ruptura de la película lagrimal.
Años despúes, en 1969, Van Bijterveld O.P. 13, realiza un pormenorizado análisis de los test diagnósticos propuestos hasta ese entonces, establece una guía de interpretación de los mismos, estadifica las manchas tincionales obtenidas mediante el rosa de bengala y sienta las bases del proteinograma lagrimal.
En 1971 se establece un concepto revolucionario hasta ese momento: el fenómeno de mojabilidad (Fig. 2). A través del mecanismo de mojabilidad, Holly F. J., y Lemp M. 14, determinan que los mucopolisacáridos presentes en el mucus epitelial son los responsables de transformar a los epitelios de la córnea y de la conjuntiva, naturalmente hidrófobos en hidrófilos.
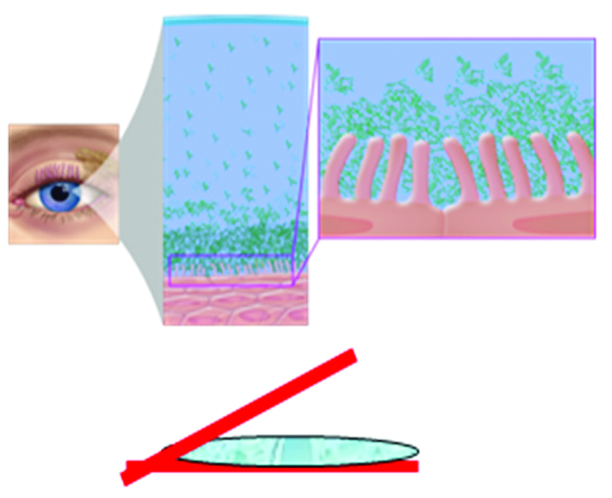
Figura 2 A: El fenómeno de mojabilidad. Con mucus: Reducción del ángulo de contacto, hidrofilia y mojabilidad.
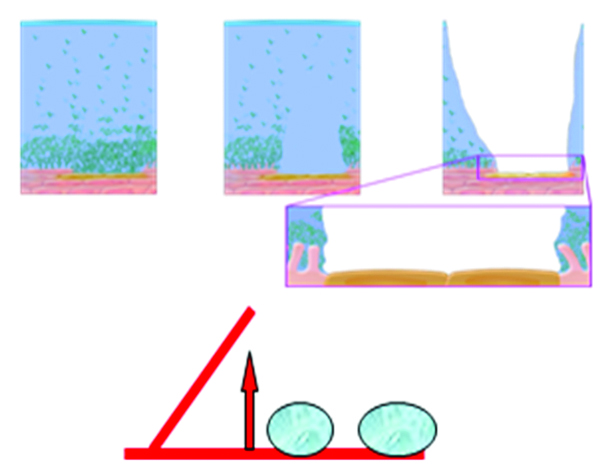
Figura 2 B: El fenómeno de mojabilidad. Sin mucus: Aumento del ángulo de contacto, hidrofobia, no mojabilidad.
Con mucus, la tensión superficial de la interfase film-epitelios disminuye el ángulo de contacto entre el film y los epitelios generando que la capa acuosa se extienda uniformemente sobre las capas celulares, permitiendo no sólo su lubricación, sino también su nutrición y sostén.
A menos concentración o con mala calidad de mucus, la tensión superficial aumenta, el ángulo de contacto entre el film y los epitelios se amplía, el film se separa de los mismos y los epitelios se hacen hidrófobos quedando expuestos a la disecación.
El fenómeno de mojabilidad y la importancia del mucus afianzan además la hasta hoy indeclinable tendencia a manejar terapéuticamente el ojo seco con lubricantes de alto contenido en polímeros mucosos hidrofílicos.
Este nuevo concepto no desvió la posición dominante que dentro de la primera ola tuvo la queratoconjuntivis sicca y el síndrome de Sjögren. En 1982, se fundó en los EE.UU. la Sjögren´s Syndrome Foundation, cuya primer presidente y socia fundadora, Elaine Harris, promovió la publicación de “The moisture seekers”, órgano de difusión de esa asociación.
Nuestro medio tampoco fue ajeno a este fenómeno. En este sentido, la fuerza de esta tendencia fue tal que en 1987, junto con un grupo de pacientes portadores de este síndrome y profesionales de la salud establecimos nexos con la Sjögren´s Syndrome Foundation.
Ese año, se realizó en Buenos Aires la primera reunión de pacientes locales y en reciprocidad con “The moisture seekers” y su socia fundadora dimos el punto de partida a la Asociación Sindrome de Sjögren Argentina (ASSA) que sigue funcionando desde ese entonces y hasta nuestros días.
Tres años después de esa reunión, y junto con la Dra. Leticia Fonseca jefa del servicio de reumatología del Hospital Rivadavia y su staff, inauguramos el primer centro de atención de pacientes portadores de síndrome de Sjögren, que también sigue brindando atención a pacientes en nuestros días.
La primera ola y la importancia del mucus promovió la publicación de uno de los más importantes tratados que sobre ojo seco tuvimos en ese entonces. La sociedad francesa de oftalmología presenta “L´oeil sec” (Fig. 3), tratado por demás completo sobre esta patología, que dedica dos capítulos completos al Síndrome de Sjögren, establece conceptos fisiopatológicos de fundamental importancia para esta patología, reafirma el concepto del mucus y el glicocalix, y establece un concepto crucial dentro de los fenómenos fisiopatológicos que involucran al ojo seco: “evaluando la cristalización de las lágrimas se observa que 50mOsm de aumento ejercidos por la glucosa, no afecta la cristalización lagrimal; pero 50mOsm de aumento ejercidos por el cloruro de sodio, afecta sensiblemente la osmolaridad”.

Figura 3: L´oeil sec
“Si una idea no parece absurda de
entrada, pocas esperanzas hay para ella”.
Albert Einstein
LA HIPEROSMOLARIDAD DEL FILM
Tomando como antecedente la descripción anteriormente mencionada, en el año 1993 publicamos en Archivos de Oftalmología de Buenos Aires (Fig. 4) nuestra hipótesis sobre la fisiopatología del ojo seco postulando un concepto que nos acompaña hasta el día de hoy: “La hiperosmolaridad del film lagrimal y el fenómeno osmótico son claves de la fisiopatología del ojo seco y de las lesiones celulares epiteliales presentes en este síndrome”.
Establecimos que el ojo seco es una condición patológica de la superficie ocular, de etiología multifactorial, donde la alteración cualicuantitativa de la película lagrimal trae aparejado una serie de fenómenos fisiopatológicos que generan circuitos viciosos de retroalimentación y cuyo correlato final es el daño epitelial por aumento de la apoptosis celular.

Figura 4: La hiperosmolaridad del film lagrimal
En el ojo seco, el descenso en la producción de lágrimas o la evaporación de las mismas incrementa rápidamente la osmolaridad del film lagrimal (Fig. 5) y disminuye la densidad de las células mucosecretantes. Las células mucosecretantes son responsables de la producción de mucus, que a expensas fundamentalmente de la Muc-5, constituye el lubricante natural de la superficie ocular. Al alterarse la cantidad y la calidad de las mucinas, aumenta la tensión superficial de la interfase epitelios-film con lo que las células epiteliales quedan expuestas al medio ambiente.
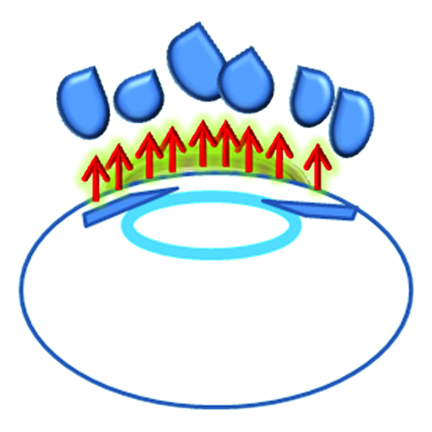
Figura 5: Fenómeno osmótico. Cambio de dirección del flujo de solventes.
El incremento del gradiente osmótico 15 entre la película lagrimal y las células epiteliales y estroma produce además un cambio direccional del fluido natural de líquidos entre estas estructuras cuyo correlato final es el aumento de la apoptosis por deshidratación, posterior descamación y daño (Fig. 6).
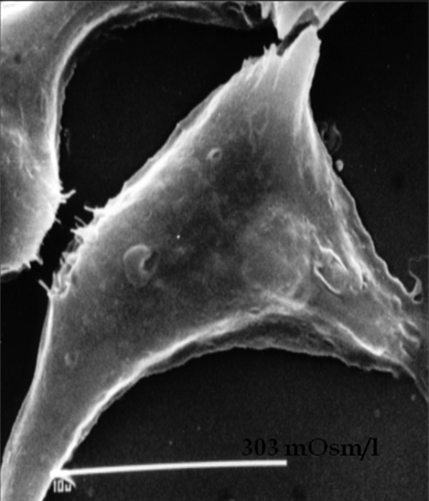
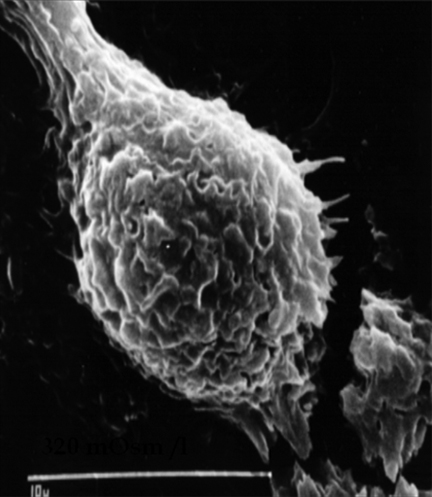
Figura 6.: Célula epitelial normal y expuesta a la hiperosmolaridad.
El desarrollo natural de la enfermedad despierta además fenómenos inflamatorios mediados por citoquinas (Fig. 7) que junto a los procesos de destrucción celular osmótica generan la pérdida de la homeostasis de la superficie ocular y daño directo celular epitelial. En este punto, los mecanismos neurofisiológicos implicados en la regulación autonómica de la superficie ocular, fallan al intentar reestablecer el orden fisiológico. Se genera un exagerado incremento del tránsito de señales neuroquímicas, que traen como consecuencia la activación de fenómenos de autoinmunidad, así como también más inflamación y por consiguiente más daño.
303 mOsm/l
600 mOsm/l 1h
600 mOsm/l 24h
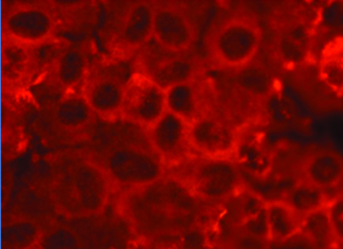
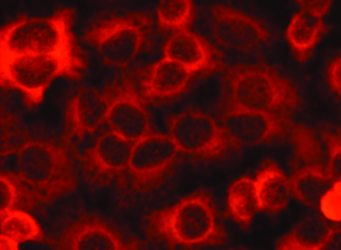
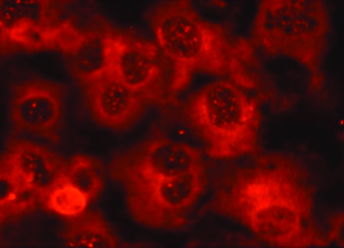
Figura 7: Hiperosmolaridad y liberación de mediadores inflamatorios 17.
La desestabilización de la superficie ocular 16 entra en este período en un proceso de retroalimentación que aumenta y cronifica la lesión sobre la superficie ocular.
Publicaciones del National Eye Institute en 1995 18 y varios años después en el International Dry Eye Work shop de 2007 19 reafirman estos conceptos.
LA SEGUNDA OLA
A partir de estos trabajos y potenciados por reuniones de la Tear film and ocular surface y su organismo de publicación “the ocular surface” comienza a darse importancia a la glándula de Meibomio y su impacto en la problemática del ojo seco 20.
Es un hecho que desde la aparición de estas sociedades científicas se han incrementado las investigaciones sobre el proceso disfuncional de estas glándulas, así como también se ha focalizado sobre la importancia de un correcto diagnóstico y mejor tratamiento de estas alteraciones.
Así como en la primera ola la queratoconjuntivitis sicca dominó la escena, la disfunción de la glándula de Meibomio toma ese rol en la actualidad, aparecen nuevos métodos de diagnóstico, nuevos equipos para su análisis y nuevas modalidades terapéuticas para su tratamiento.
Como ya mencionáramos, el desarrollo en conceptos clave sobre el ojo seco evidenciado en la primera ola, no tiene comparación con el de la segunda ola; mucho menos prolífica y de escaso desarrollo hasta la fecha desde ese punto de vista.
MÉTODOS DIAGNÓSTICOS 21
Sin ningún lugar a dudas, el examen biomicroscópico bajo la lámpara de hendidura es el primer paso en la evaluación diagnóstica del ojo seco.
La evaluación del menisco lagrimal y de las características anatómicas y funcionales de la superficie ocular es fundamental en el desarrollo de los pasos diagnósticos de la enfermedad.
Debe incluirse además el examen biomicroscópico de los párpados y anexos palpebrales, así como también de la arquitectura de la superfcie ocular.
La tríada clásica (por mí denominada eterna) compuesta por el test de Schirmer, las tinciones y el BUT nos acompañan hasta nuestros días (Fig. 8).
El test de Schirmer simplemente nos muestra un papel de filtro mojado por las lágrimas y no suministra otro valor. Un ojo mojado no es sinónimo de que esté lubricado, es más, muchos pacientes portadores de ojo seco presentan epífora como síntoma y hasta llegan a empapar la bandeleta de papel del test de Schirmer.
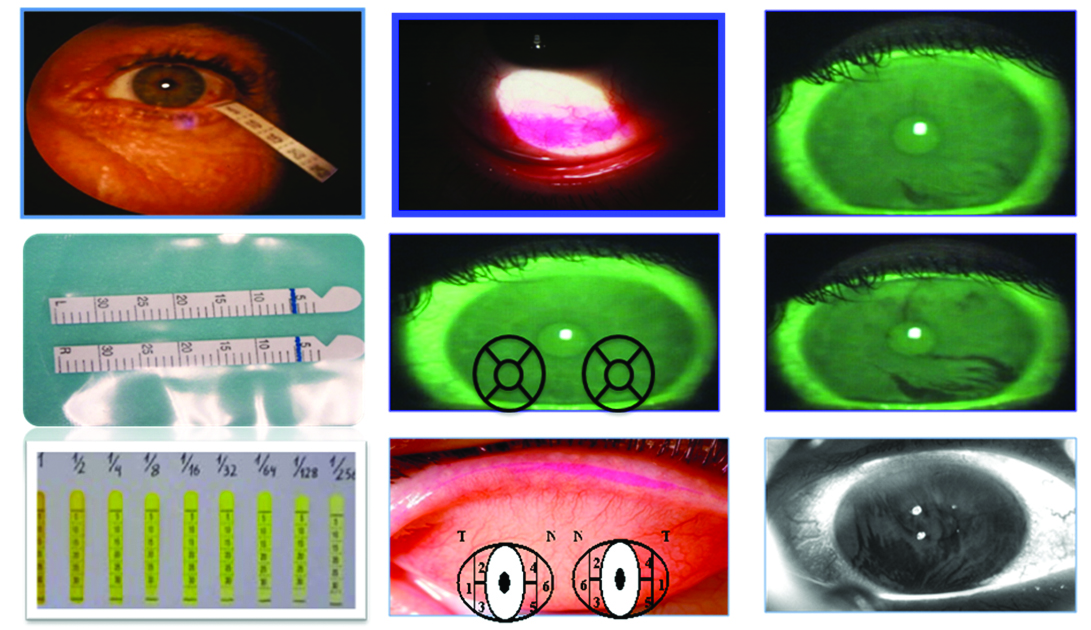
Figura 8: La tríada eterna
El test de Schirmer puede ser útil comparando el nivel de humidificación basal con el nivel de humidificación luego del estímulo nasal, y de esta manera inferir el grado de respuesta reflejo de la glándula lagrimal, esto es útil en pacientes portadores de colagenopatías, donde las glándulas exócrinas están alteradas por la infiltración linfoplasmocitaria típicas de esos cuadros.
Cobra importancia al permitir evaluar el aclaramiento lagrimal o clearence lagrimal, lo que permite evaluar la dinámica de la película lagrimal y darnos una imagen aproximada del grado inflamatorio de la superfcie ocular por mayor o menor concentración de elementos inflamatorios.
La tinción con fluoresceína o solución de Grant permite evaluar la superficie epitelial de la córnea y determinar la presencia o no de soluciones de continuidad y lesiones.
Dividimos la córnea en cinco cuadrantes y según el grado tincional le otorgamos un valor de cero a tres, al mismo tiempo que podemos diferenciar macro o micropuntillado sobre la córnea.
La tinción con rosa de bengala o lisamina verde sobre la superficie epitelial conjuntival determina la presencia o no de mucus. Dividimos la conjuntiva en seis cuadrantes y le otorgamos al grado tincional un valor de cero a tres para su evaluación.
Estos dos colorantes permiten diferenciar los cuadros lacrimodeficientes de cuadros evaporativos según tiñan la zona expuesta o la zona no expuesta conjuntival.
Con el rosa de bengala o la lisamina verde se puede determinar además el grado de fricción palpebral que se expresa al evertir el párpado superior y observar si el colorante tiñe el borde interno palpebral (Fig. 9).
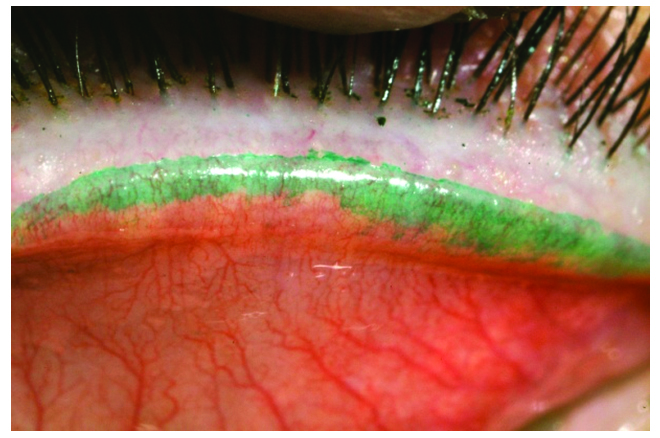
Figura 9: Tinción con lisamina zona de fricción
El tiempo de ruptura de la película lagrimal brinda una vasta información sobre el grado de exposición de la superficie epitelial córneo-conjuntival independientemente del tiempo de ruptura propiamente dicho. Si la ruptura de la película lagrimal es acompañada por un correcto parpadeo, la superficie ocular estará protegida, por más que el valor del BUT medido en segundos sea bajo. Por el contrario, si la ruptura en segundos no se acompaña de un acompasado parpadeo, la superficie ocular estará desprotegida, por más que los segundos medidos se encuentren dentro de lo establecido.
De esta manera, el BUT permite evaluar la integración del eje superficie ocular, sistema nervioso central, párpados.
Cobra importancia además el determinar la zona donde se produce la primera imagen de sequedad y muy especialmente si la misma se produce en el eje visual.
El método tradicional para realizarlo es con instilación de cantidades estandarizadas de fluoresceína o solución de Grant. En la actualidad, existen equipos como el Tearscope (Fig. 10) o el Keratograph (Fig. 11) que permiten realizarlo sin el uso de esos colorantes. A esta forma de realizarlo se le denomina BUT no invasivo.

Figura 10: Tearscope
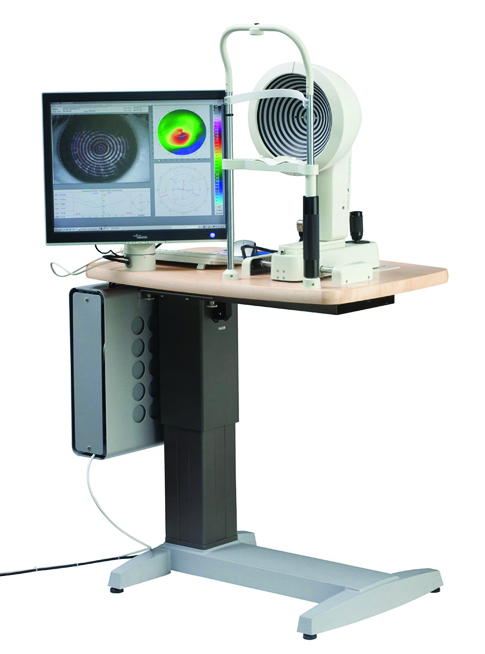
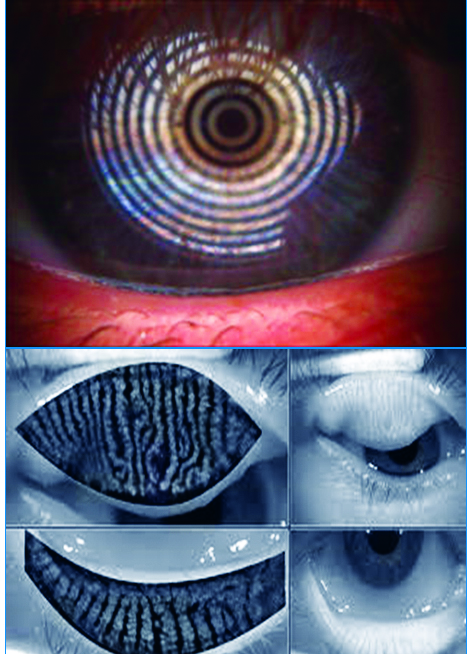
Figura 11: Keratograph. Imágenes tomadas de la web
del equipo.
Ambos equipos evalúan eficazmente al menisco lagrimal y a su capa lipídica, y el Keratograph realiza además un muy eficaz análisis de las glándulas de Meibomio.
Nuevos y sofisticados equipos como el HD analyzer (Fig. 12) analizan el film lagrimal y la calidad visual en función al tiempo transcurrido entre parpadeos. Básicamente establece el grado de recuperación o no de la visión a medida que el ojo está expuesto al medio ambiente y hasta el momento del parpadeo. En ese instante, si la película lagrimal se encuentra estable, la calidad visual debe recuperarse; por el contrario si la película lagrimal es inestable, pese al parpadeo la calidad visual no se recupera.

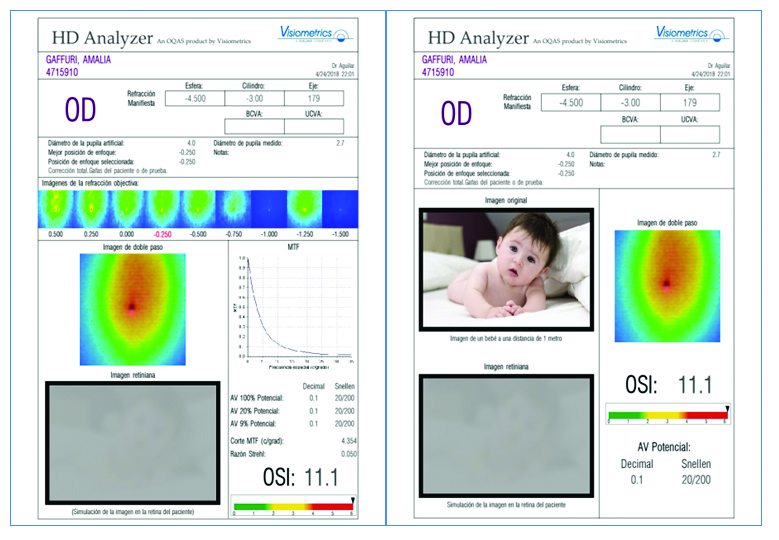
Figura 12: HD Analyzer
La dispersión de la imagen retineal en relación a la dinámica del film lagrimal en y durante el parpadeo constituye un punto de vital importancia para evaluar la inclusión o no de un paciente a cirugía refractiva o facorrefractiva o para evaluar en el post quirúrgico el grado de impacto o no del film lagrimal en la calidad visual.
El equipo analiza además pormenorizadamente los principales aspectos de la glándula de Meibomio y mide con exactitud de manera no invasiva el BUT.
Sin lugar a dudas el poder evaluar eficazmente la osmolaridad de la película lagrimal es el test por el cual tendríamos la certeza diagnóstica de ojo seco. Si bien existen en la actualidad equipos dirigidos al oftalmólogo (Fig. 13). Estos dispositivos realizan la medición mediante un microchip electrónico por lo que no evalúan específicamente osmolaridad, sino que mide la oposición eléctrica de carga, es decir impedanciometría eléctrica. De esta manera no son lo suficientemente certeros para evaluar la osmolaridad lagrimal.
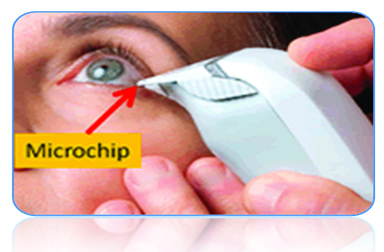
Figura 13: Osmómetros oftalmológicos. Imagen tomada de la web.
Sus resultados presentan diferencias sustanciales al compararlos con los complejos y sofisticados microosmolímetros de precisión que establecen con certeza el valor en miliosmoles.
Una forma indirecta de avaluar osmolaridad es medir el contenido de sodio presente en el film lagrimal. En este sentido, el papel de filtro del test de Schirmer al absorber fluido lagrimal, absorbe también sodio y de la misma manera que se realiza el test del sudor para la mucovisidiosis, se puede realizar esa evaluación.
Si bien la liberación de citoquinas es una consecuencia secundaria del aumento de la osmolaridad del film, su evaluación es útil para el manejo terapéutico, para decidir en qué momento ocluir los puntos lagrimales o para incluir o no a un paciente en prequirúrgico refractivo. La evaluación de mediadores inflamatorios requiere de sofisticados equipos para realizarlo, pero en la actulaidad existe un kit diagnóstico, “inflamma dry” (Fig. 14) que a semejanza de los conocidos test de embarazo, evalúa la presencia o no de metaloproteinasas en superficie ocular. No permite su cuantificación.
El laboratorio de superficie ocular es otro aliado fundamental para el diágnóstico de esta enfermedad.
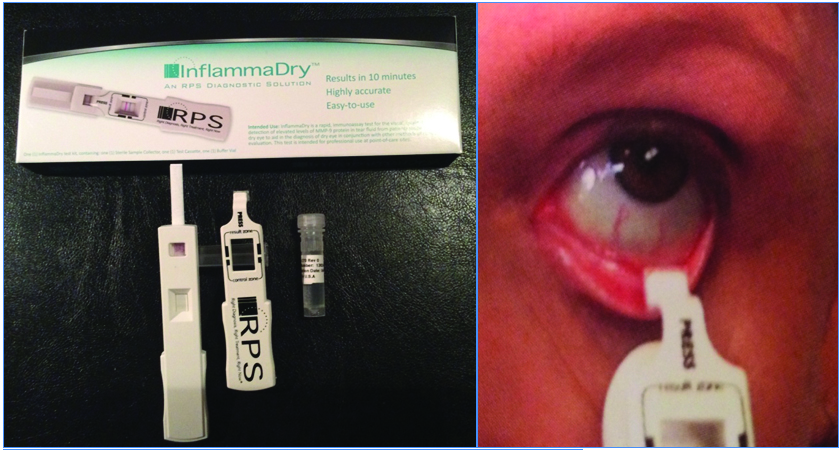

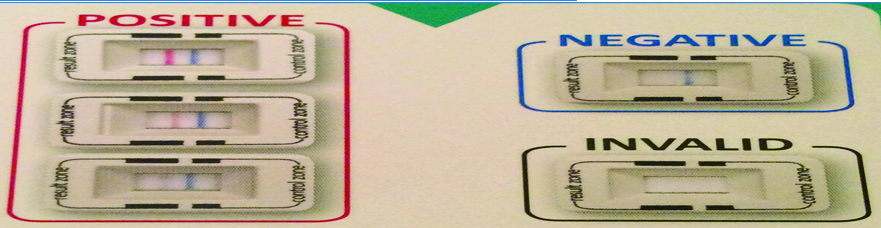
Figura 14: Inflamma dry
El proteinograma lagrimal evidencia tres fracciones en la corrida electroforética (Fig. 15). La primera fracción está determinada por la albúmina sérica y proteínas de migración rápida; la segunda fracción está determinada por la lactotransferrina e inmunoglobulinas (IgE, A,G y M) y la tercera fracción está conformada en su totalidad por la Lisozima, enzima de capacidad antibiótica que suele disminuir cuando está afectada la glándula lagrimal.
La citología de impresión (Fig. 16) permite identificar los cambios metaplásicos experimentados por la superficie epitelial conjuntival como consecuencia del ojo seco e identificar las características histológicas de las células mucosecretantes y de otras células que conforman a la superficie epitelial conjuntiva.

Figura 15: Proteinograma lagrimal
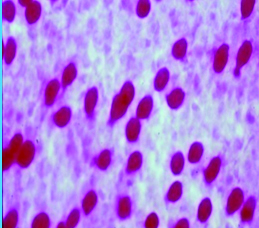
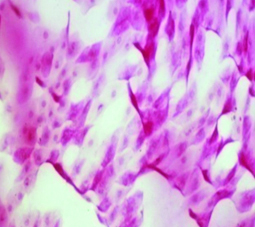
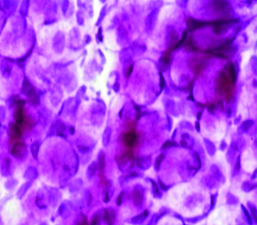
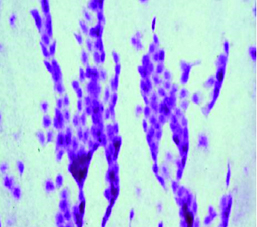
Figura 16: Citología de impresión
Permite diferenciar cuadros de ojo seco, de alergia, de disfunción de glándula de Meibomio, de toxicidad y realizar un correcto diagnóstico diferencial. Estudios comparativos con biopsia labial de pacientes portadores de Síndrome de Sjögren 22 le dan un gran valor diagnóstico de esa enfermedad.
Es de gran utilidad para diagnosticar disfunciones límbicas.
Estudios más complejos de laboratorio como la inmunohistoquímica (Fig. 17) sobre tejido conjuntival obtenido por biopsia permite el diagnóstico de certeza del penfigoide ocular cicatrizal al identificar depósitos de IgG, IgM y Complemento 3 en membrana basal.
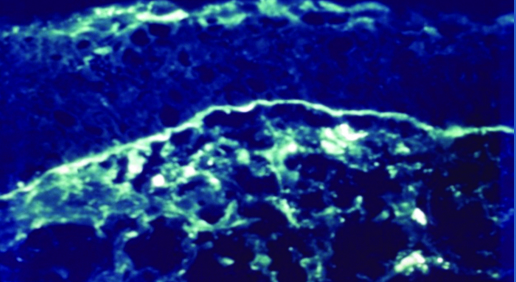
Figura 17: Inmunohistoquímica
TRATAMIENTOS
1) Sustitutivo:
Se basa en la sustitución del mucus epitelial con soluciones lubricantes mucomiméticas que permiten estabilizar transitoriamente al film lagrimal, equilibrar la interfase epitelios-film y mejorar el daño celular epitelial.
Sus formas de presentación son en colirio, gel o ungüento oftálmico, y tienen la capacidad de aumentar el tiempo de retención de la lágrima.
Pueden presentarse además en forma sólida, para ser aplicados en el fondo del saco conjuntival inferior, desde donde se disuelven lentamente otorgando un efecto más prolongado y duradero. Son denominados “inserts” (Fig. 18).

Figura 18: Inserts
Las soluciones lubricantes se formulan a base de polímeros hidrofílicos de diferentes características fisicoquímicas. Los tres grandes grupos farmacológicos son: derivados de la celulosa, derivados polivinílicos y polisacáridos.
Si bien no son formulaciones sustitutivas, cabe mencionar dentro de este apartado, el manejo farmacológico con liposomas en spray, que en uso paralelo a los lubricantes pueden contribuir a mejorar los signos y síntomas del ojo seco.
2) Tratamiento estimulante:
A través del uso de agentes estimulantes secretorios o secretagosos se puede obtener un aumento de la secreción de las distintas capas que componen el film lagrimal.
– Estimulantes de la secreción lipídica: civamide
– Estimulantes de la secreción acuosa: pilocarpina oral, bromexina y n-acetil cisteína; estos últimos de acción mucolítica paralela.
– Estimulantes de la secreción mucosa: rebamipide, ecabet, diquafosol.
3) Tratamiento trófico:
Consiste en la utilización de agentes con capacidad de favorecer o activar la nutrición y regeneración del tejido epitelial dañado.
Dentro de este grupo se encuentran el calostro, el suero autólogo, la vitamina A (local y sistémica), la nandrolona y la trealosa.
4) Tratamiento inmunomodulador/antiinflamatorio:
El disminuir la actividad del linfocito T y su capacidad de estimular el proceso inflamatorio, se ha constituido en la actualidad en una valiosa herramienta dentro del manejo terapéutico del ojo seco.
Dentro de este grupo encontramos: ciclosporina (0.05-1%), tacrolimus, pimecrolimus, anacrinas y lifitegrast.
Como agentes antiinflamatorios: los esteroides de superficie, fluorometolona, rimexolona y loteprednol.
En mi experiencia personal desaconsejo los aines.
El uso de tetraciclinas orales puede ofrecer la ventaja de brindar un efecto antiinflamatorio secundario, así como también los suplementos dietarios como el ácido omega 3; hoy en revisión.
Todas estas soluciones anteriormente descriptas están generalmente preservadas con conservadores, cuyo análisis merece un capítulo aparte, ya que muchos de ellos pueden provocar daño directo celular epitelial. En este sentido, dentro del grupo de los conservadores más frecuentemente utilizados en las formulaciones lubricantes, el Cloruro del Benzalconio (BAK) es uno de los más agresivos para la superficie ocular, y por lo tanto el que debemos evitar.
Su acción tóxica sobre la superficie epitelial, así como también su efecto detergente sobre la capa lipídica del film son dos de sus principales desventajas.
5) Tratamiento quirúrgico:
El tratamiento quirúrgico se enfoca específicamente en la reparación del posible daño severo que el ojo seco y generalmente sus patologías sistémicas asociadas pudieran haber provocado sobre la superficie ocular (Fig. 19).
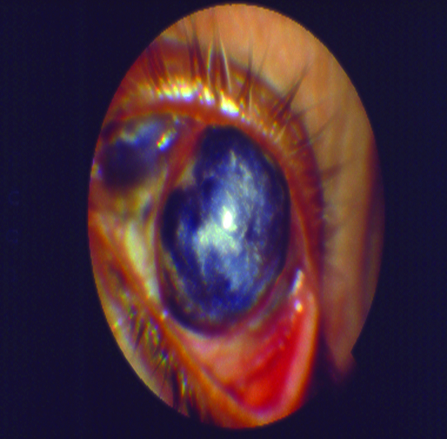
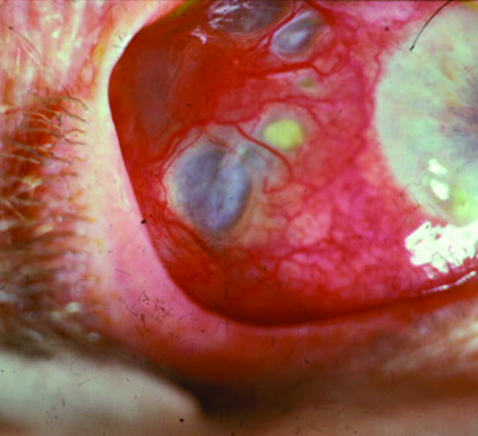
Figura 19: Daño severo de la superficie ocular
Dentro del tratamiento quirúrgico se encuentran los injertos de limbo, los injertos de amnios y las queratoplastias.
Cabe mencionar la posibilidad de disponer de tejido amniótico en forma directa para aplicar sobre la superficie ocular que la empresa Biotissue tiene disponible. Este dispositivo denominado “Prokera” (Fig. 20) encierra el tejido amniótico dentro de dos anillos que a modo de lente de contacto se aplica directamente sobre el ojo.

Figura 20: Prokera. Imagen tomada de la web
6) Tratamiento biotecnológico:
Consiste en la aplicación sobre la superficie ocular de nuevas tecnologías que favorecen la normal funcionalidad de las glándulas de Meibomio. Dentro de este grupo encontramos dispositivos que contribuyen al drenaje y limpieza de los párpados (Fig. 21) como: blephex, blephasteam, lipiflow y luz pulsada).
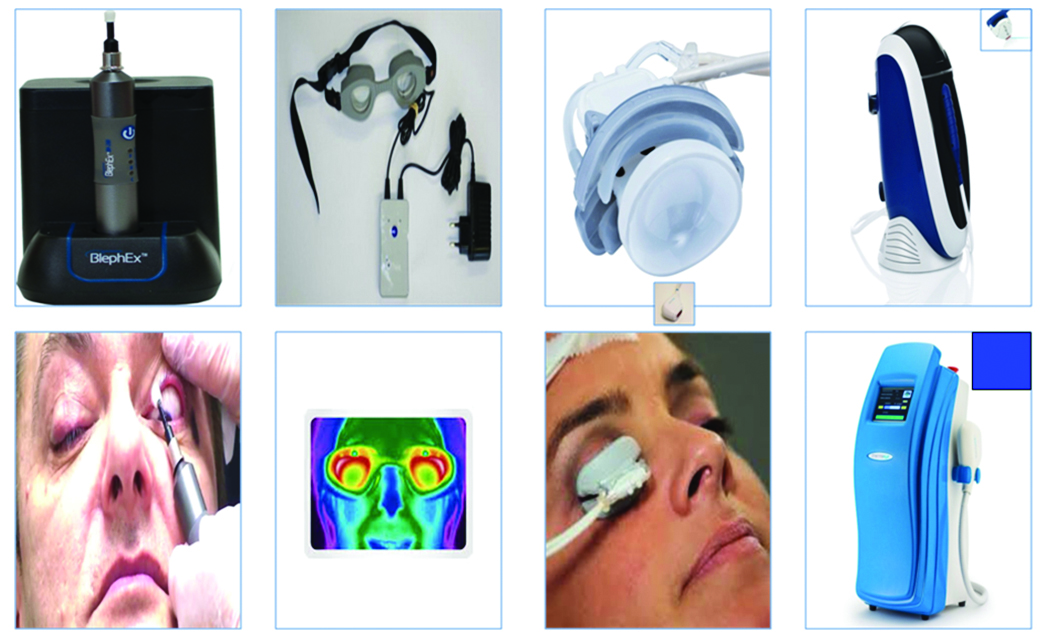
Figura 21: Biotecnología. Imágenes tomadas de la web de los equipos
7) Tratamiento oclusivo:
La oclusión de los puntos lagrimales con tapones lagrimales o implantes intracanaliculares son ampliamente utilizados para el manejo del ojo seco y ayudan a disminuir la osmolaridad de la película lagrimal.
En mi experiencia y opinión personal, sostengo hace largo tiempo que el uso de los denominados tapones lagrimales de silicona pueden agravar los cuadros inmunológicos y/o inflamatorios presentes en el ojo seco, al fomentar los fenómenos inmunocompentes por fricción sobre la superfcie ocular (Figs. 22, 23, 24).
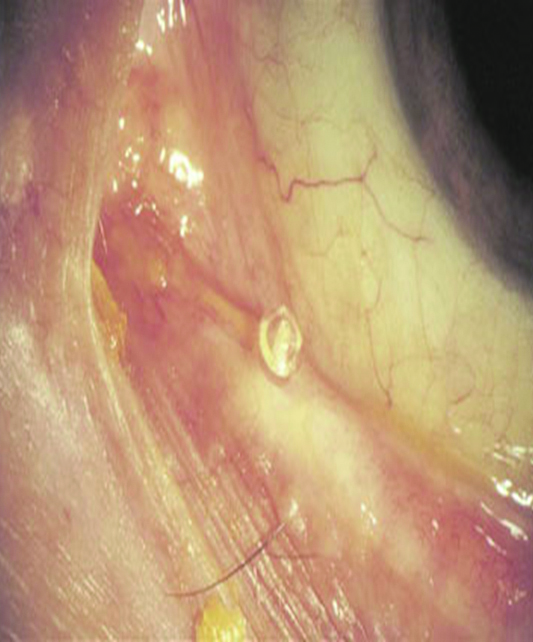
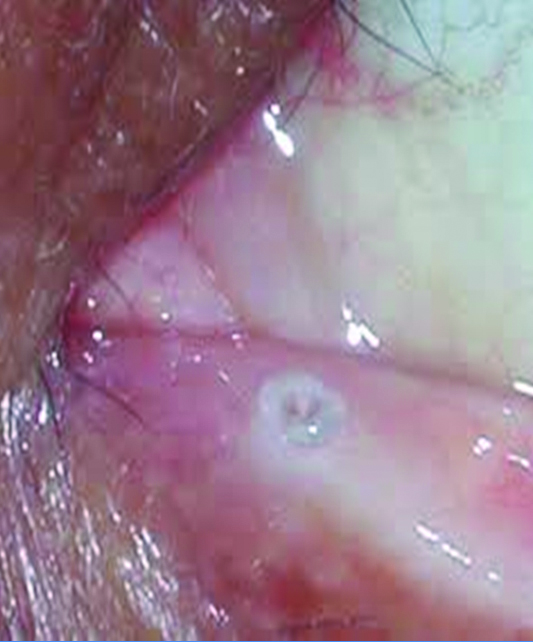
Figura 22: Borde del tapón lagrimal sobre la superficie conjuntival y acúmulos secretorios secundarios.
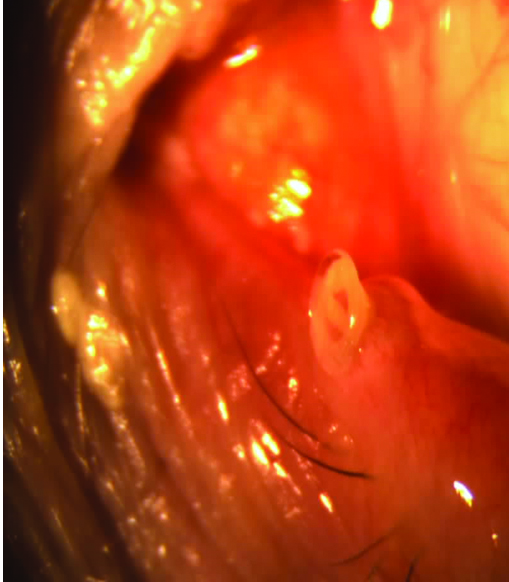
Figura 23: Borde del tapón deteriorado friccionando la superficie ocular. Secreción, congestión y edema conjuntival.
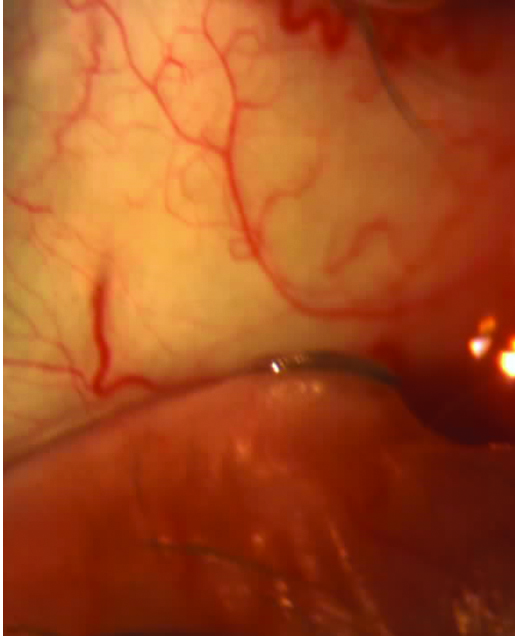
Figura 24: Contacto del tapón lagrimal en conjuntiva.
Sostuve y sostengo también, que esa fricción crónica puede estimular a los linfocitos conjuntivales y en pacientes susceptibles desencadenar fenómenos de tipo linfoides.
Ambas presunciones han sido recientemente informadas (REF).
Es por ese motivo que prefiero el uso de implantes intracanaliculares profundos de uso extendido o de hidrogel.
He comprobado además en mi práctica que al retirar los tapones lagrimales, los mismos se encuentran con su arquitectura totalmente degradada en un alto porcentaje de los casos (Fig. 25).
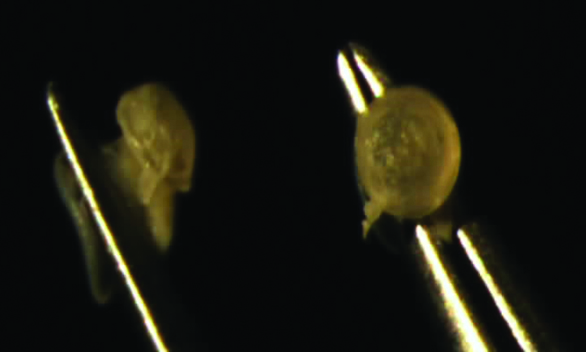
Figura 25: Tapón degradado.
Otro factor a tener en cuenta dentro de la problemática del uso de los tapones lagrimales es el cambio anatómico que se produce en la estructura del punto lagrimal. Dilatación, edema, reacciones papilares, inflamación y fibrosis son frecuentes hallazgos (Fig. 26).
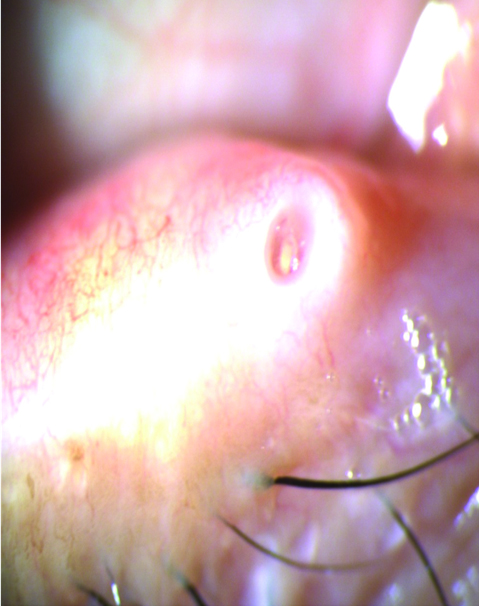
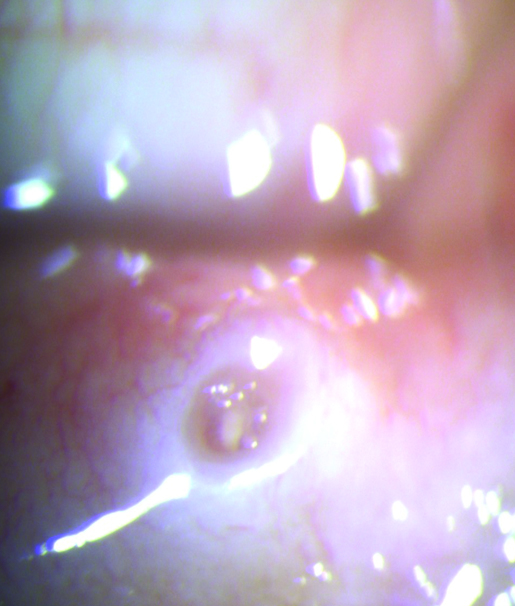
Figura 26: Cambios anatómicos en el punto lagrimal al retirar los tapones.
8) Tratamiento con lentes de contacto:
El uso de lentes de contacto terapéuticas está indicado en casos de ojo seco con lesiones erosivas o ulcerativas recurrentes de córnea.
En la actualidad, el reemplazo del uso de las lentes terapéuticas clásicas por el grupo de lentes esclerales (Figs. 27 y 28) ha contribuido a mejorar su efecto terapéutico.

Figura 27: Lente de contacto escleral. Imagen cedida por la Licenciada Carmen E. Ferraris.
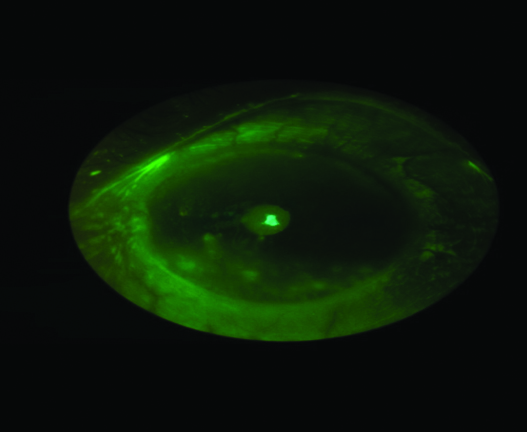
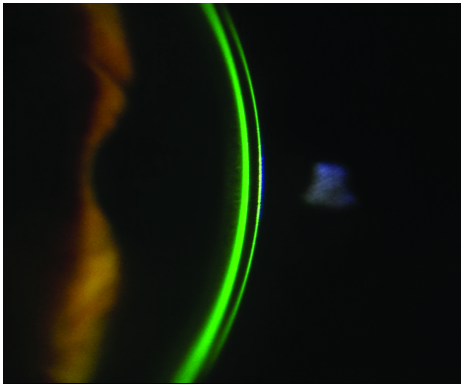
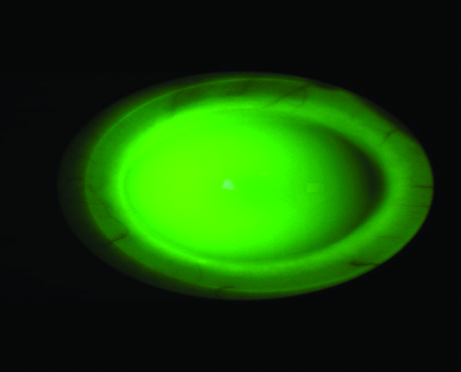
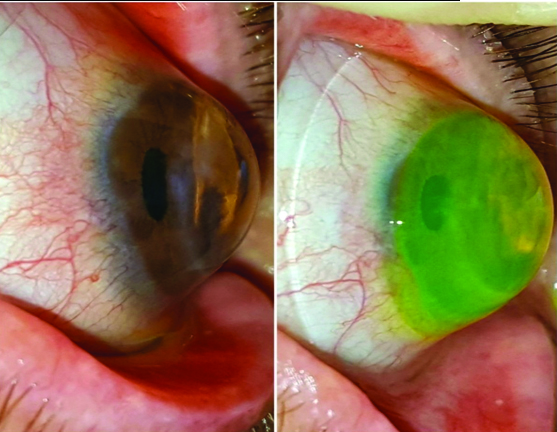
Figura 28: Lente de contacto escleral. Imagen cedida por la Licenciada Carmen E. Ferraris.
Las características funcionales de este tipo de lente de contacto hacen posible además la concentración de las drogas vehiculizadas en forma de colirio, ya que las mismas se retienen entre la superficie epitelial y la cara interna de la lente escleral, potenciado el efecto y actuado además como reservorio de lágrimas.
9) Tratamiento ambiental:
El manejo de las condiciones ambientales resulta indispensable para mejorar la calidad de vida del paciente con ojo seco. En este sentido, el mejorar las condiciones de humedad ambiente, y alertar al paciente sobre los factores que pueden disparar o agravar su condición es de gran valor para contribuir a una mejor respuesta terapéutica.
Limitar la exposición a monitores de computación, tv, aire acondicionado excesivo, fuentes de calor, viento y sol, así como también hacer consciente al paciente del parpadeo.
Lentes de protección o las denominadas cámaras húmedas son de gran utilidad para mantener adecuados niveles de film lagrimal y evitar su evaporación.
10) Nuevos horizontes:
En los últimos tiempos hemos estado trabajando en la incorporación del uso medicinal del cannabis para tratar las afecciones inflamatorias e inmunológicas de la superficie ocular con resultados muy satisfactorios y auspiciosos.
El estímulo de los receptores conjuntivales cannabinoides, así como también de los receptores distribuidos por el resto del organismo puede contribuir al manejo de estas enfermedades y quizás en un futuro ser un aliado esencial en el manejo terapéutico de estas patologías.
HIPEROSMOLARIDAD
El ojo seco es un trastorno común de la superficie ocular, de gravedad variable, que afecta a cientos de millones de personas en todo el mundo. Cerca de 5 millones de estadounidenses mayores de 50 años presentan ojo seco severo 1, 2, 3. Se estima que en los Estados Unidos, el gasto social atribuible al ojo seco es de 3.800 millones de dólares/año en costos directos de la atención y de 55.000 millones/año en costos indirectos por pérdida de productividad 1.
En nuestro país, a prevalencia, incidencia y gastos en salud aún no ha sido estimados, sin embargo, es sabido que es la segunda causa de consulta oftalmológica luego de la prescripción de lentes y, que la venta de lubricantes oculares (lágrimas artificiales) y fármacos para su tratamiento es la franja que más creció en los últimos 10 años en el mercado farmacéutico de oftalmología.
En 1992, trabajos realizados conjuntamente entre los Dres. Aguilar y Berra, mostraron la relación entre hiperosmolaridad y transformación del fenotipo del epitelio conjuntival humano. Encontramos que la hiperosmolaridad lagrimal lleva a una disminución de las células caliciformes
y a un cambio en el fenotipo de las células epiteliales (fenotipo metaplásico) (Fig. 29).
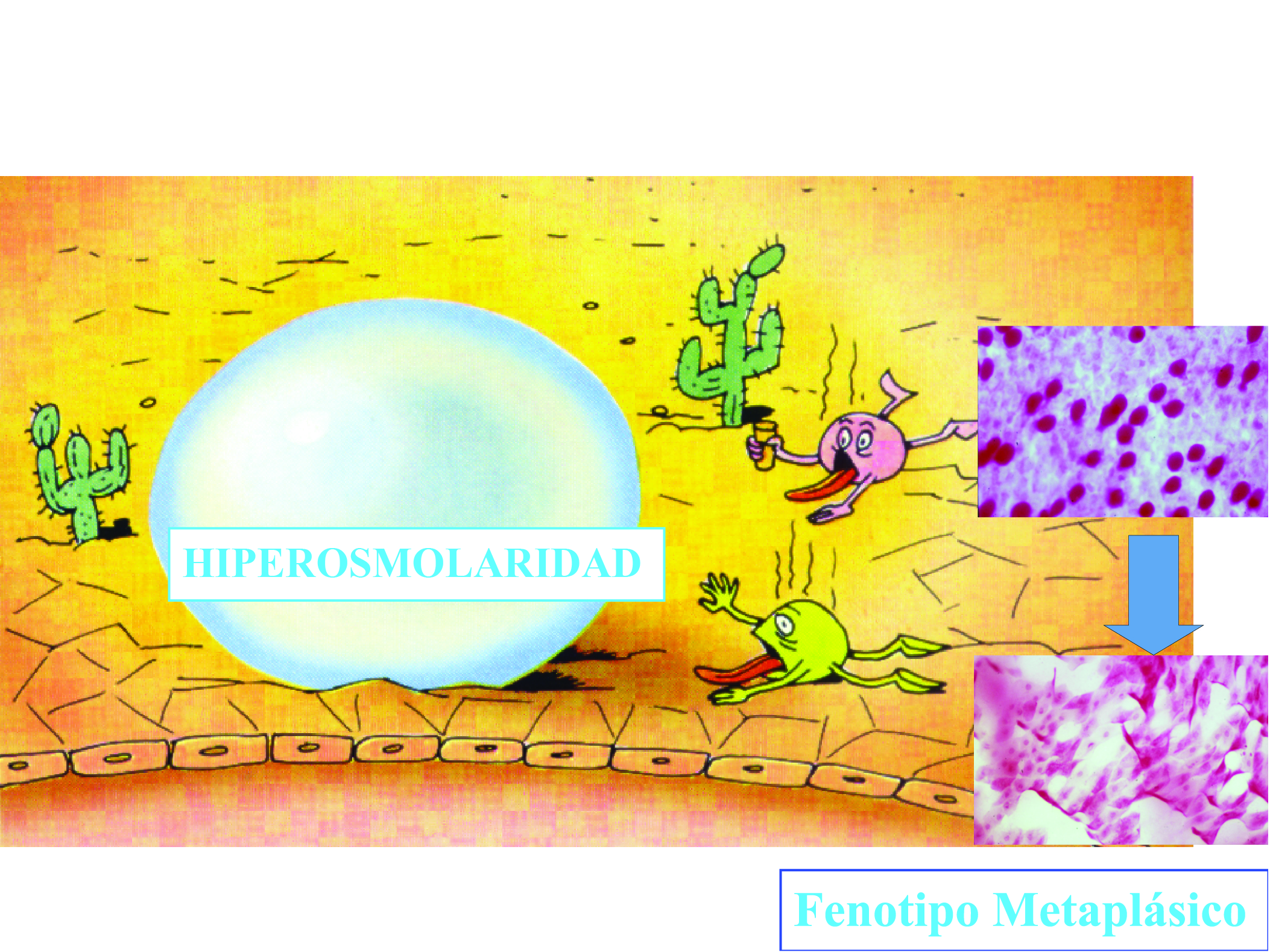
Figura 29: Relación entre hiperosmolaridad con el ojo seco y fenotipo metaplásico.
Un incremento significativo en la osmolaridad lagrimal se ha asociado con el ojo seco desde hace décadas4, 5. El estrés producido por la hiperosmolaridad en pacientes con ojo seco induce la secreción de citoquinas proinflamatorias también ha sido reportado desde hace décadas6, 7, 8, 9.
El informe Dry Eye Workshop II de la International Society of Tear Film and Ocular Surface (TFOS DEWS II 2017) elaborado por más de 150 representantes de sociedades científicas y universidades de 23 países definió al ojo seco como “una enfermedad multifactorial de la superficie ocular caracterizada por la pérdida de la homeostasis de la película lagrimal y acompañada por síntomas oculares, en los que la inestabilidad de la película lagrimal donde la hiperosmolaridad, la inflamación y el daño de la superficie ocular desempeñan papeles etiológicos” 10 (Fig. 30). El mismo informe centra a la hiperosmolaridad lagrimal como el eje central de un círculo vicioso donde la hiperosmolaridad, por evaporación o déficit en la producción, activa las vías de MAPk y NF-ΚB que inducen la producción diversas citoquinas proinflamatorias (IL- 1ß, IL-6, IL-17, IFN -γ, TNF-α), las células epiteliales e inestabilidad de la película lagrimal11.
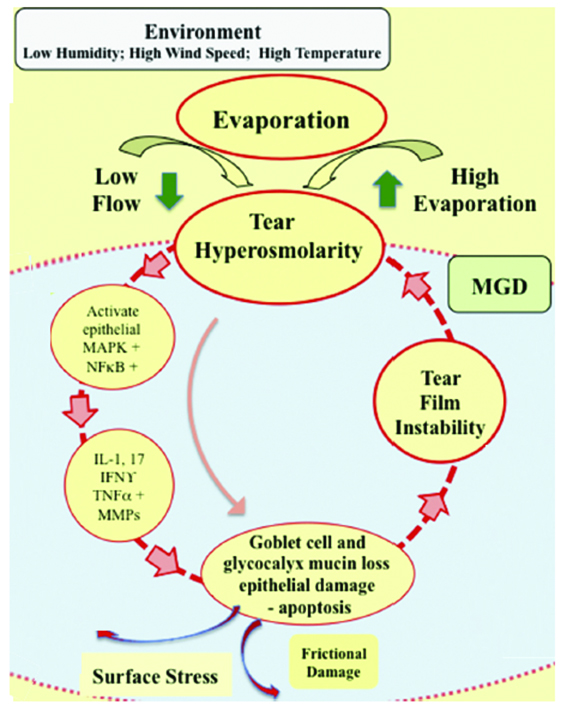
Figura 30
Nuestro grupo fue el primero en mostrar este círculo vicioso en 2005. Nosotros evaluamos pacientes con ojo seco severo por Síndrome de Sjögren (panel izquierdo), ojo seco moderado (panel central) e individuos normales (panel derecho), allí mostramos que los pacientes Síndrome de Sjögren presentaban osmolaridad lagrimal mayor a 340 mOsm/l, ausencia de células caliciformes y fenotipo metaplásico en las células epiteliales. La hiperosmolaridad lagrimal lleva a una clara translocación nuclear del factor NF-ΚB. Por el contrario, los individuos normales, presentan osmolaridad lagrimal menor a 320 mOsm/l, con cantidad normal de células caliciformes, células epiteliales sin metaplasia y ausencia de traslocación nuclear del factor NF-ΚB (Fig. 31).

Figura 31: Asociación entre hiperosmolaridad, fenotipo metaplásico
y translocación nuclear del factor NF-κß
En 2006, nuestro grupo mostró este círculo vicioso en estudios in vitro en células epiteliales de conjuntiva (Fig. 32).
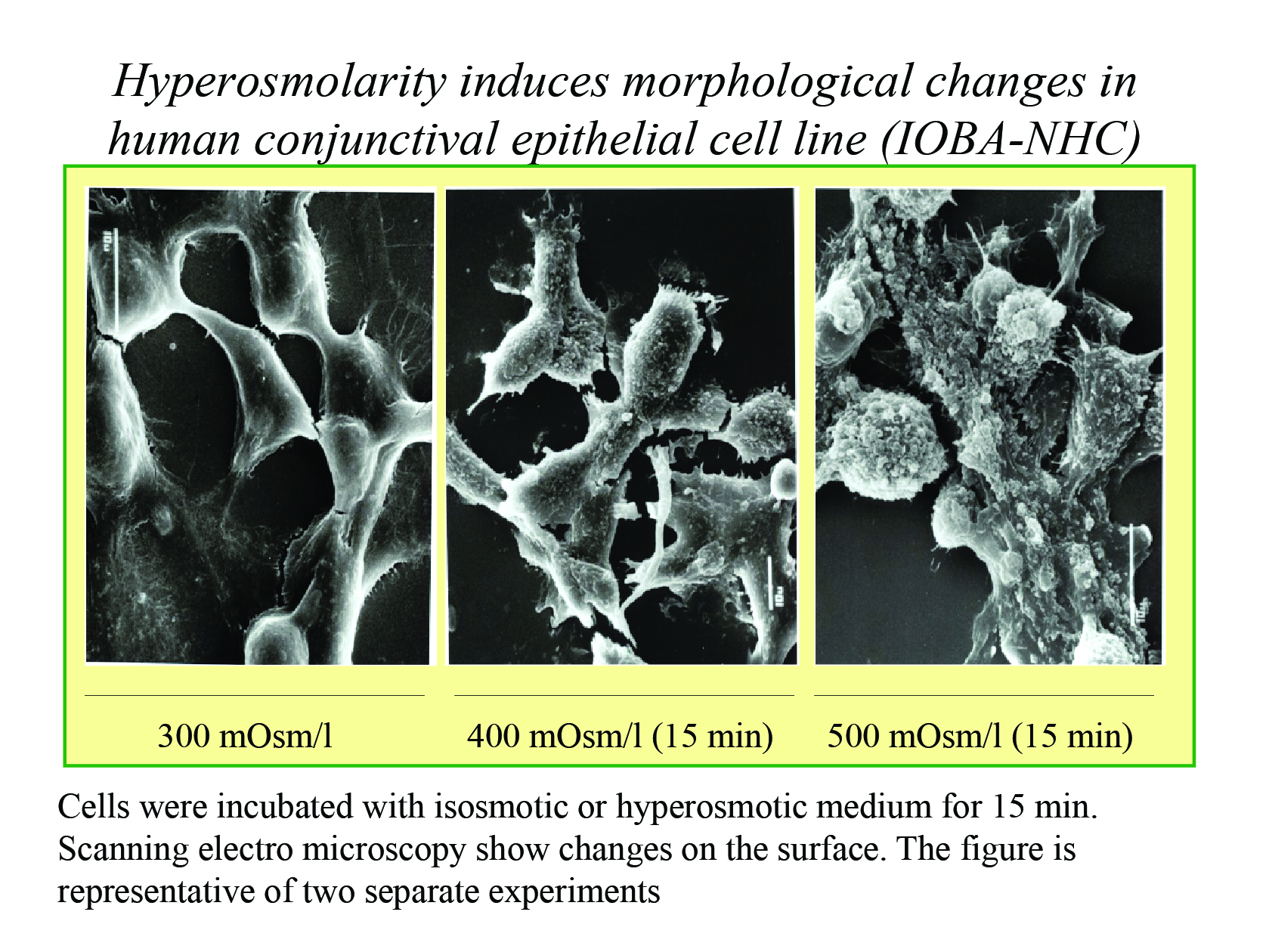
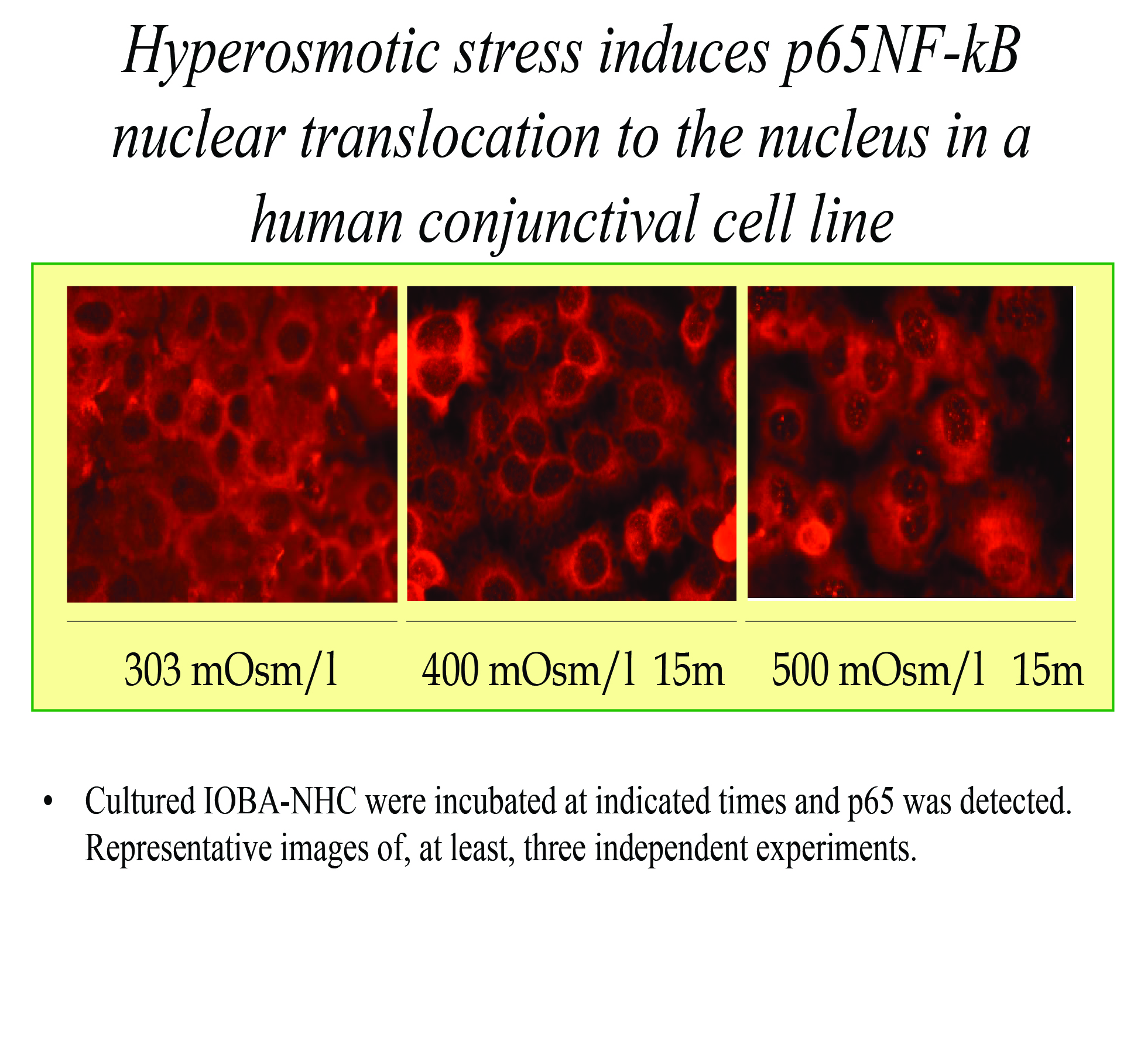
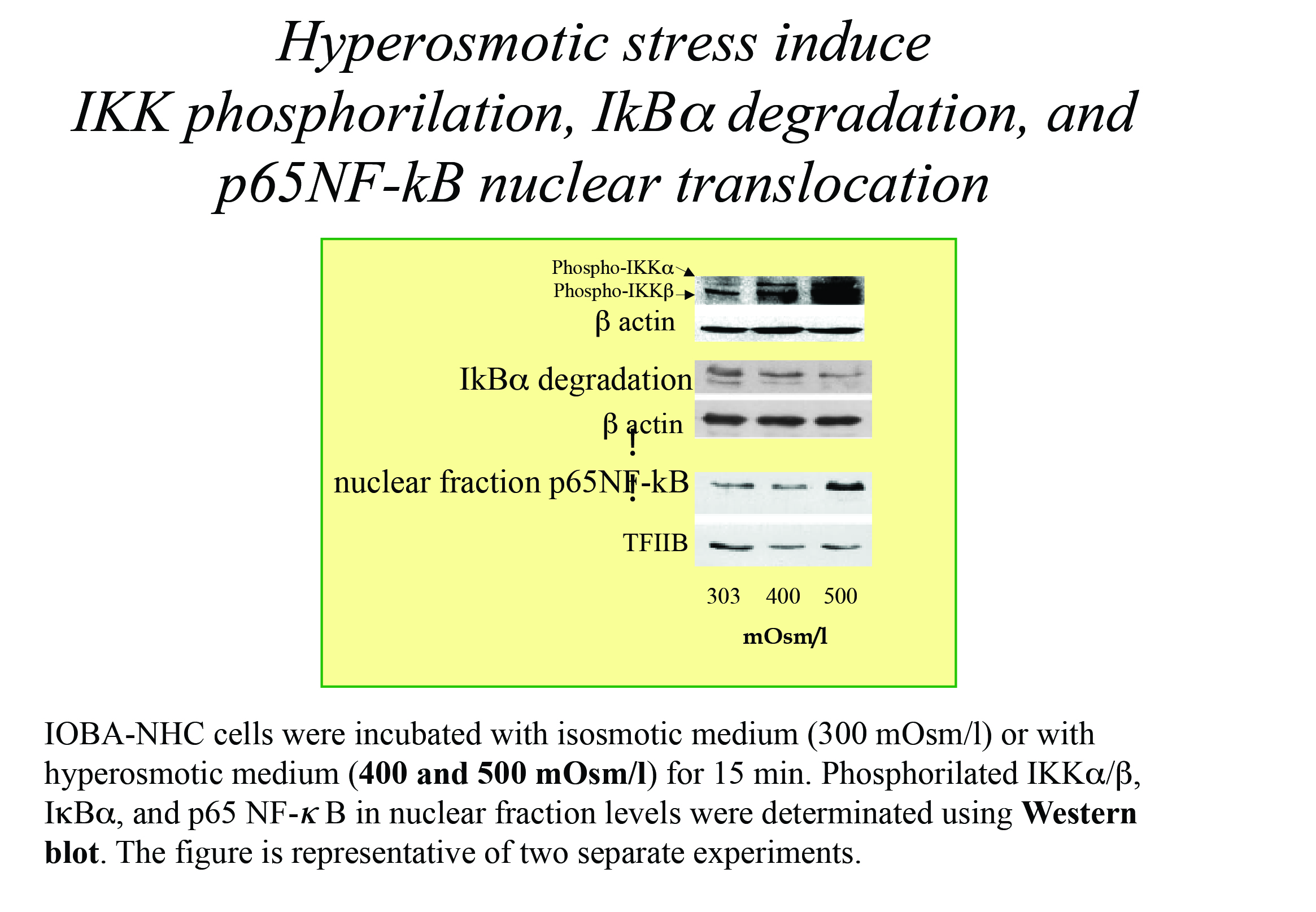

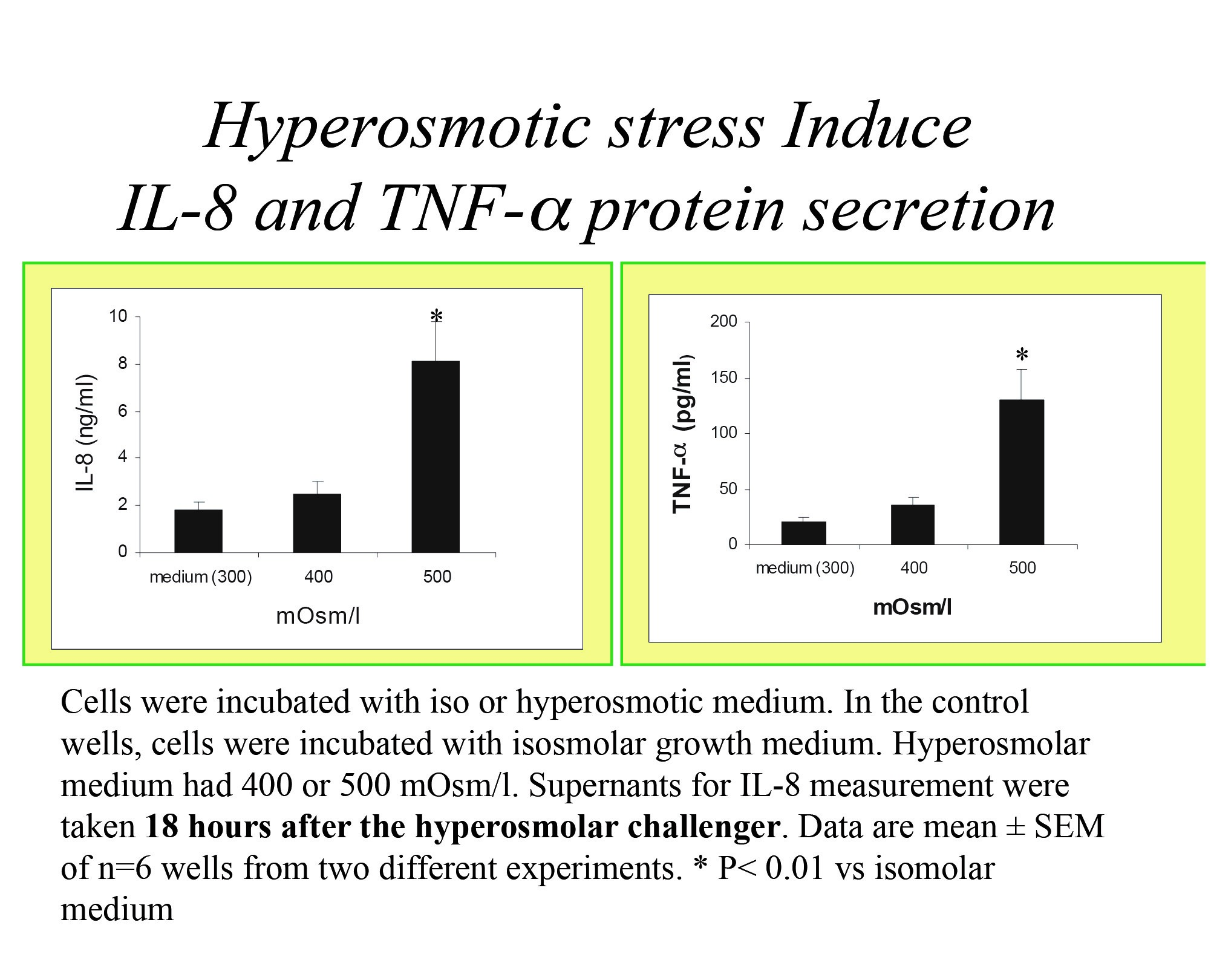

Figura 32
CONTAMINACIÓN AÉREA
Actualmente la contaminación aérea de megaciudades afecta a millones de individuos a nivel mundial, produciendo inequívocas oculares. Hasta el momento se toma a la contaminación aérea de megaciudades como un factor ambiental que exacerba al ojo seco y no como productor de conjuntivitis por si mismo.
Los contaminantes aéreos que comúnmente se encuentran en el aire de los centros urbanos son gases y partículas en suspensión tales como, el monóxido de carbono (CO), los óxidos de nitrógeno y azufre (NOx, SOx), los hidrocarburos aromáticos policíclicos (HAPs), los polifenoles clorados (PCBs), metales pesados y material particulado (MP) 12, 13, 14, 15. Lya contaminación ambiental aérea depende entre otros factores de la geografía, el clima y las fuentes de emisión, siendo el impacto sobre la salud específico y único para cada
megaciudad. En particular, el efecto adverso del MP sobre la salud depende de su composición química (Ej. presencia de metales, PCBs, HAPs), tamaño aerodinámico (≤2,5 um; 5-10 um y ≥10 um) y forma, siendo éstas características reflejo de la actividad antropogénica distintiva de cada megaciudad.
Se sabe que Buenos Aires representa la ciudad con mayor cantidad de habitantes de Argentina, en donde, habitan aproximadamente 3 millones de personas en 200 km2 de superficie. Si consideramos el área metropolitana de Buenos Aires (AMBA) constituida por la ciudad y 24 distritos del conurbano, esta cifra asciende a 15 millones de habitantes y constituye el décimo conglomerado mundial.
Nosotros propusimos y demostramos que el efecto de la contaminación ambiental sobre la superficie ocular, presenta el mismo círculo vicioso. Al igual que el ojo seco, que la exposición al aire de megaciudades lleva a la activación de las vías de MAPk (ERK/JNK) y NFΚB16 e inducción en la producción diversas citoquinas proinflamatorias (IL-1ß, IL-6, IFN -γ, TNF-α) 17, 18, 19, 20, 21, 22, 23 (Fig. 33).
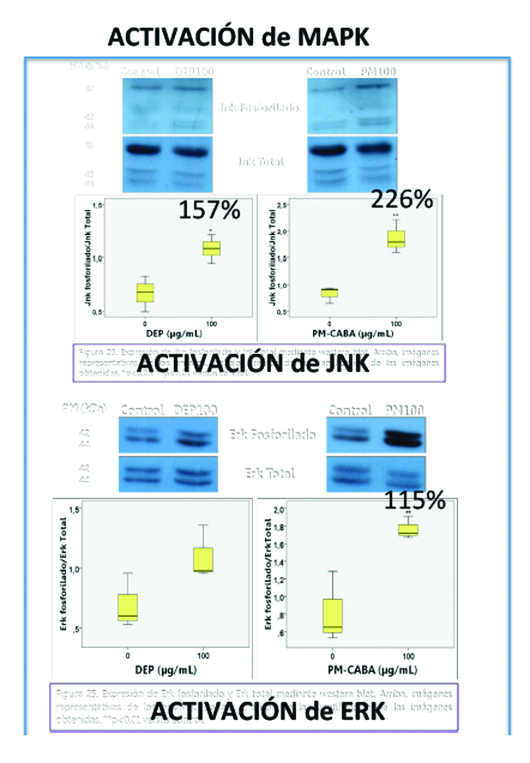
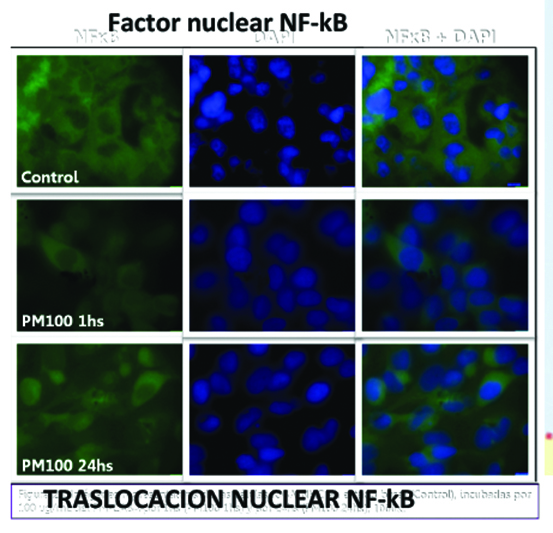
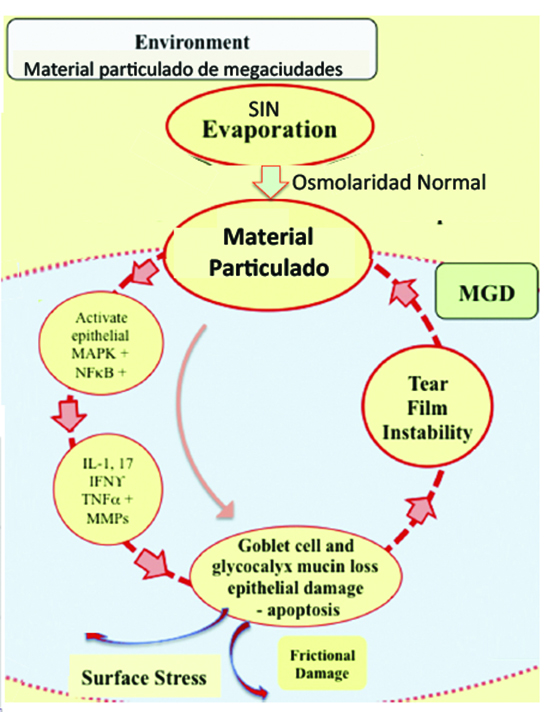
Figura 33
EFECTO DE LA CONTAMINACIÓN AÉREA SOBRE EL BUT
Para corroborar que el BUT se asociaba a la contaminación ambiental realizamos un estudio epidemiológico en áreas de extremadamente baja contaminación ambiental (Parque Nacional Los Glaciares y El Chalten), bajos (Río Grande y Ushuaia) y medios/altos (Buenos Aires) encontramos una correlación inversa entre niveles de contaminación ambiental y tiempo de ruptura de la película lagrimal. El promedio de BUT fue de 14,5 seg. en Parque Nacional Los Glaciares; 10,8 seg en Río Grande; 11,1 seg. en Ushuaia y 7,1 seg. en Buenos Aires. Para destacar fue que algunos guardaparques en Parque Nacional Los Glaciares tuvieron BUT cercanos a 20 seg. (Fig. 34).
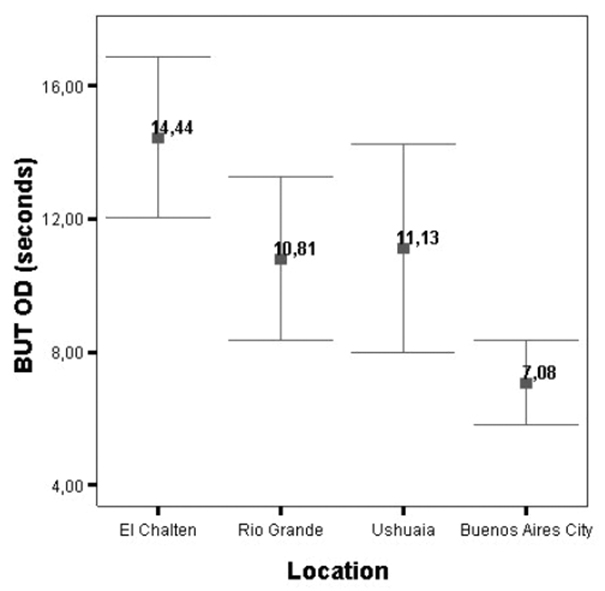

Figura 34
En estos trabajos intervinieron varios oftalmólogos que sin su ayuda desinteresada hubiera sido imposible realizar este trabajo, ellos son: En Parque Nacional Los Glaciares: Dres. Pablo Gruccio y Martin Berra; en Ushuaia: Dr. Cristina Aguado y; en Buenos Aires: Dres. Alejandro Aguilar, Martín Berra y Rafael Iribarren.
EFECTO DE LA CONTAMINACIÓN AÉREA AGUDA DE ORIGEN ANTROPOGÉNICO. CASO 1
En abril 2008, la quema de pastizales en la zona de Zárate, Buenos Aires y la dirección del viento hizo que el Área Metropolitana de Buenos Aires (AMBA) donde habitan y trabajan más de 14.000.000 habitantes se viera afectada por el humo proveniente de dicha quema de pastizales. En la imagen de la derecha arriba se observa la imagen satelital del 18 de abril de 2008, y abajo la imágenes del Obelisco en pleno centro de la ciudad de Buenos Aires, a la izquierda en el día de la fecha y a la derecha luego a los 6 meses de la quema de pastizales (Fig. 35).
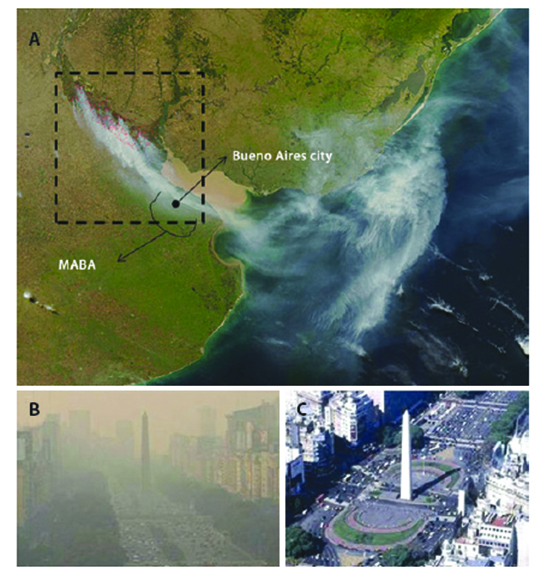
Figura 35: A) Satellite image (MODIS/Aqua) of the wildfires in the Delta of the Parana River on April 18th, 2008. Red boxes indicate wildfire areas. Scale: 1px=250m (NASA. Fires and smoke over Argentina, seen from MODIS on the Aqua satellite at 20081090418/Argentina. A200810.1750.250 m.jpg, 2008). B and C) Images of the same location in the city of Buenos Aires at two different moments. (B) April 18th, 2008, during the wildfires in the Delta of the Parana River (http://nidodecaranchosblogspot.com/2008_04_01_archive.html). (C) May 20th, 2008 (http://cliobuenosaires.blogspot.com/2010/05/el-obelisco-un-simbolo-que-define.html).
Evaluamos conjuntamente con los Dres. Gustavo Galperín y Martín Berra a pacientes que concurrieron a la guardia del Hospital Oftalmológico Pedro Lagleyze (G1) y acompañantes normales de los pacientes (G2). Las evaluaciones en ambos grupos (G1 y G2) fueron realizadas el 19 de abril de 2008, durante el periodo agudo, y luego de un mes de haberse disipado el humo (Fig. 36).
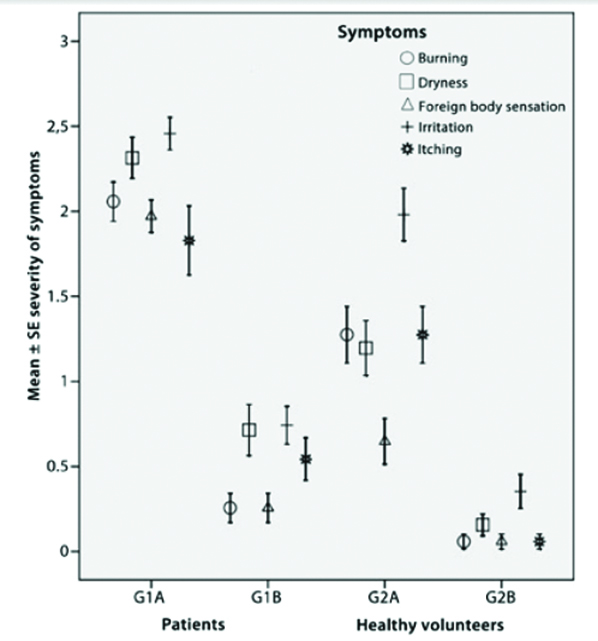
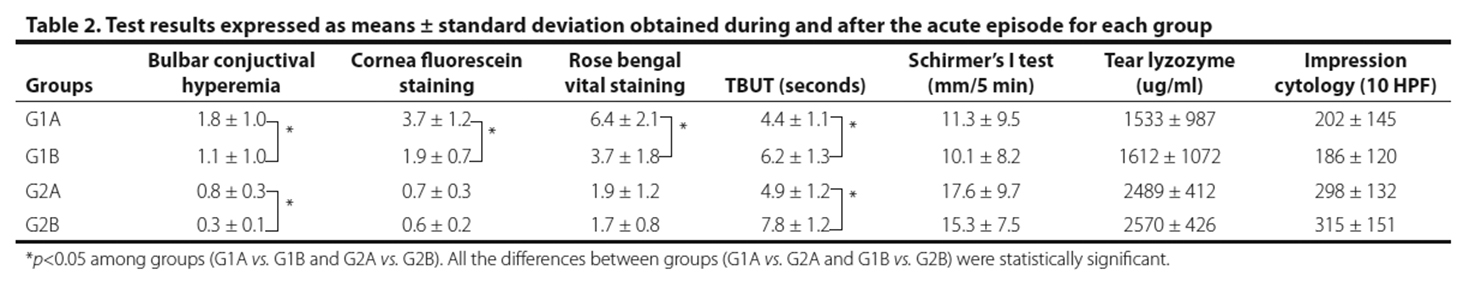
Figura 36: Severity of symptoms during and after the acute episode. The figure depicts the mean grade of the reported symptoms ± the standard deviation of the mean for each of the two groups at two different time points [during (19th of April) and after the episode (22nd of May)]. G1A = patient data during the episode; G1B = patient data after the episode; G2A = healthy volunteers data during the episode; G2B = healthy volunteers data after the episode.
Los pacientes con afecciones de la superficie ocular presentaron síntomas de quemazón, sequedad, sensación de ojo seco irritación (G1A), mientras que lo más representativo de los voluntarios sanos fue la irritación ocular (G2A). Luego de la desaparición del humo los pacientes presentaban sobre todo síntomas de irritación y sequedad, eso fue debido a su enfermedad de base (G1B), mientras que los voluntarios normales no mostraron ninguna secuela en sus síntomas.
Los pacientes del G1 presentaron en el período agudo (G1A) respecto a la posterior evaluación cuando ya no había humo en AMBA (G1B): hiperemia conjuntival, coloración positiva corneal, rosa de bengala positivo y BUT disminuido. En los voluntarios normales sólo hubo cambios significativos en el BUT.
Table 1. Study population

Table 1. Test results expressed as means ± standard deviation obtained during and after the acute episode for each group
EFECTO DE LA CONTAMINACIÓN AÉREA AGUDA DE ORIGEN ANTROPOGÉNICO. CASO 2
El 4 de junio de 2011, se produjo la erupción del volcán Puyehue en Chile. Rápidamente por el efecto de los vientos la nube volcánica cruzó la cordillera y cenizas precipitaron en las ciudades argentinas de Villa La Angostura, Bariloche. A las 48hs de la erupción la acumulación de cenizas volcánicas en estas ciudades fue cercana a los 40 cm. La columna de cenizas volcánicas duró varias semanas. Las cenizas volcánicas también afectaron fuertemente a las provincias argentinas de Chubut, Río Negro y Neuquén, llegando las ciudades de Buenos Aires y Montevideo. La nube de cenizas forzó a las aerolíneas a cancelar vuelos locales e internacionales por varios meses en el aeropuerto de Bariloche y varias semanas en el de Neuquén y Buenos Aires. Se estima que más de cien millones de toneladas de cenizas fueron expulsadas. La concentración y tamaño de las cenizas fue mucho mayor en el área de Villa La Angostura y Bariloche que en el AMBA. Las cenizas del volcán Puyehue afectaron a toda la población de Patagonia sur, sin embargo en el AMBA, las cenizas fueron de menor tamaño y concentración. Conjuntamente con el Dr. González Valdes en Bariloche y el Dr. Aguilar en AMBA estudiamos el efecto de la contaminación del volcán Puyehue en ambas ciudades. En Bariloche el Dr. González Valdes estudió a 22 individuos que vivían en el área de Bariloche (80 a 150 km del volcán) y el Dr. Aguilar a 274 individuos que habitaban en AMBA (1700 km del volcán). Nuestros resultados en el área de Bariloche relevaron que las cenizas afectaron a todos los individuos evaluados, con o sin patologías previas de superficie ocular, sin embargo, en AMBA sólo consultaron los que presentaban afecciones previas de la superficie ocular (ojo seco evaporativo y lacrimosecretor, penfigoide, alergia).
En las imágenes se observa la erupción del volcán, la imagen satelital de la pluma volcánica y fotografía de Villa La Angostura y Buenos Aires (Fig. 37).

Figura 37
En todos los casos el BUT estuvo sustancialmente disminuido durante el período agudo respecto a lo evaluado luego del mismo. La evaluación de la superficie ocular en los individuos normales del área de Bariloche no tuvieron consecuencias sobre la salud ocular en la población luego de la exposición aguda a las cenizas del volcán, de la misma manera, en aquellos pacientes estudiados en AMBA que ya poseían afecciones previas (ojo seco, alergia ocular, penfigoide, etc.) tampoco influyó sobre el curso de su patología ocular luego de la exposición aguda.
El 22 de abril de 2015, las cenizas de otro volcán ubicado en Chile, volcán Calbuco, afectó la Patagonia sur argentina, afectando varias ciudades entre ellas, Villa La Angostura, Bariloche y otras en esa área.
Nosotros evaluamos a las cenizas de las erupciones de los volcanes Puyehue (2011) y Calbuco (2015) obtenidas en Villa La Angostura (Fig. 38).
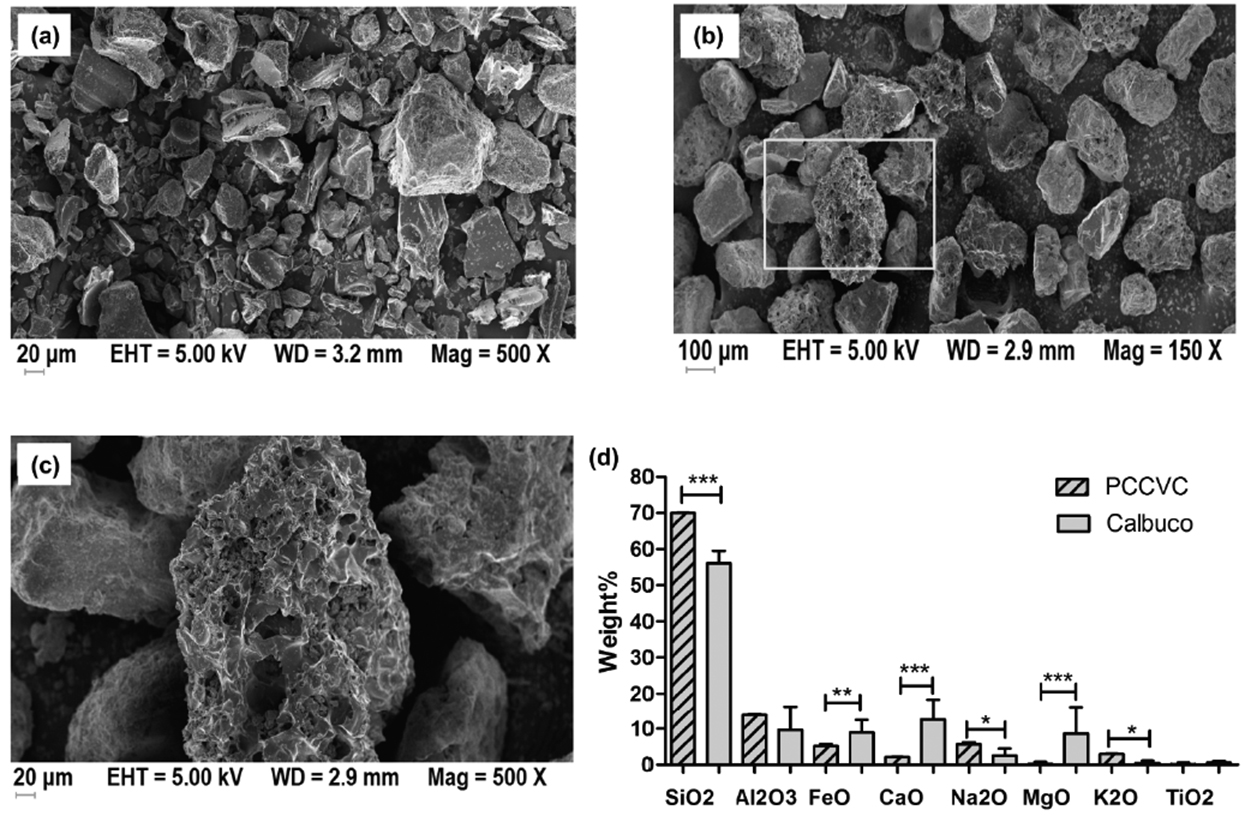
Figura 38:. Representative SEM images of PCCVC (a) and Calbuco (b) ash samples collected in Villa la Angostura. (c) shows a magnification of Calbuco particles from the yellow square in (b). (d) Ash oxide composition of PCCVC and Calbuco ash estimated after EDX elemental analysis. Results are expressed as mean values ± SEM of total weight percentage of at least three ash samples. **p<0.01, *p<0.05, *** p<0.001 by t-test.
Las cenizas del volcán Puyehue fueron heterogéneas presentando un tamaño entre 10 y 100 µm. La microscopía electrónica de scanning reveló que las del Calbuco tenían una distribución básicamente de dos tipos, unas menores a 10 µm y otras de entre 100 y 300 µm.
La composición química por microscopía electrónica EDAX también mostró diferente composición: las cenizas del Puyehue tuvieron más SiO2, Na2O y K2O (p<0,05) pero menos FeO, CaO, MgO (p<0,01).
Las cenizas del volcán Puyehue afectaron la proliferación de las células del epitelio de conjuntiva humana normal de manera exposición-dependiente, no hubo cambios en las cenizas del volcán Calbuco. Las cenizas de ambos volcanes no indujeron apoptosis o necrosis (Fig. 39).
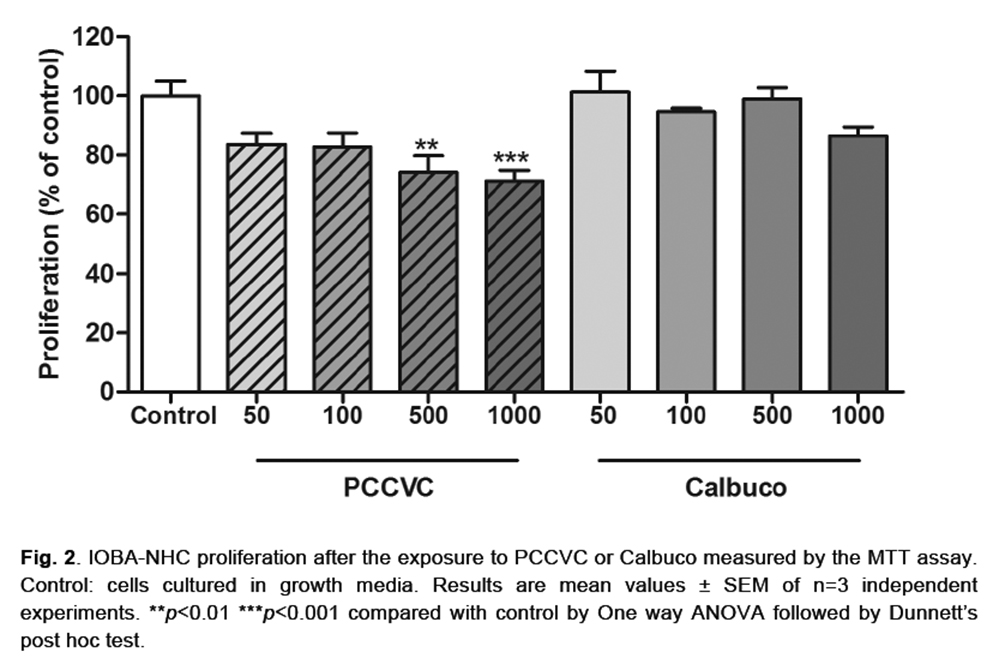
Figura 39: IOBA-NHC proliferation after the exposure to PCCVC or Calbuco measured by the MTT assay. Control: cells cultured in growth media. Results are mean values ± SEM of n=3 independent experiments. **p<0.01 ***p<0.001 compared with control by One way ANOVA followed by Dunnett’s post hoc test.
Las mucinas son glicoproteínas de alto peso molecular, componentes esenciales de la película lagrimal que eliminan los desechos y los patógenos nocivos del entorno externo y también facilitan la lubricación. Las mucinas se pueden dividir en dos subfamilias, 1) las mucinas secretadas y 2) las mucinas ligadas a la membrana. Nosotros evaluamos impacto de la contaminación del aire por fuentes naturales, en este caso por las cenizas de los volcanes Puyehue y Calbuco, en la superficie ocular. Nosotros estudiamos la expresión de la mucina ligada a membrana MUC-1. Encontramos que las cenizas del Puyehue disminuyeron la secreción de MUC-1 de manera exposición-dependiente. En contraste, las del Calbuco no mostraron cambio de actividad significativa (Fig. 40).

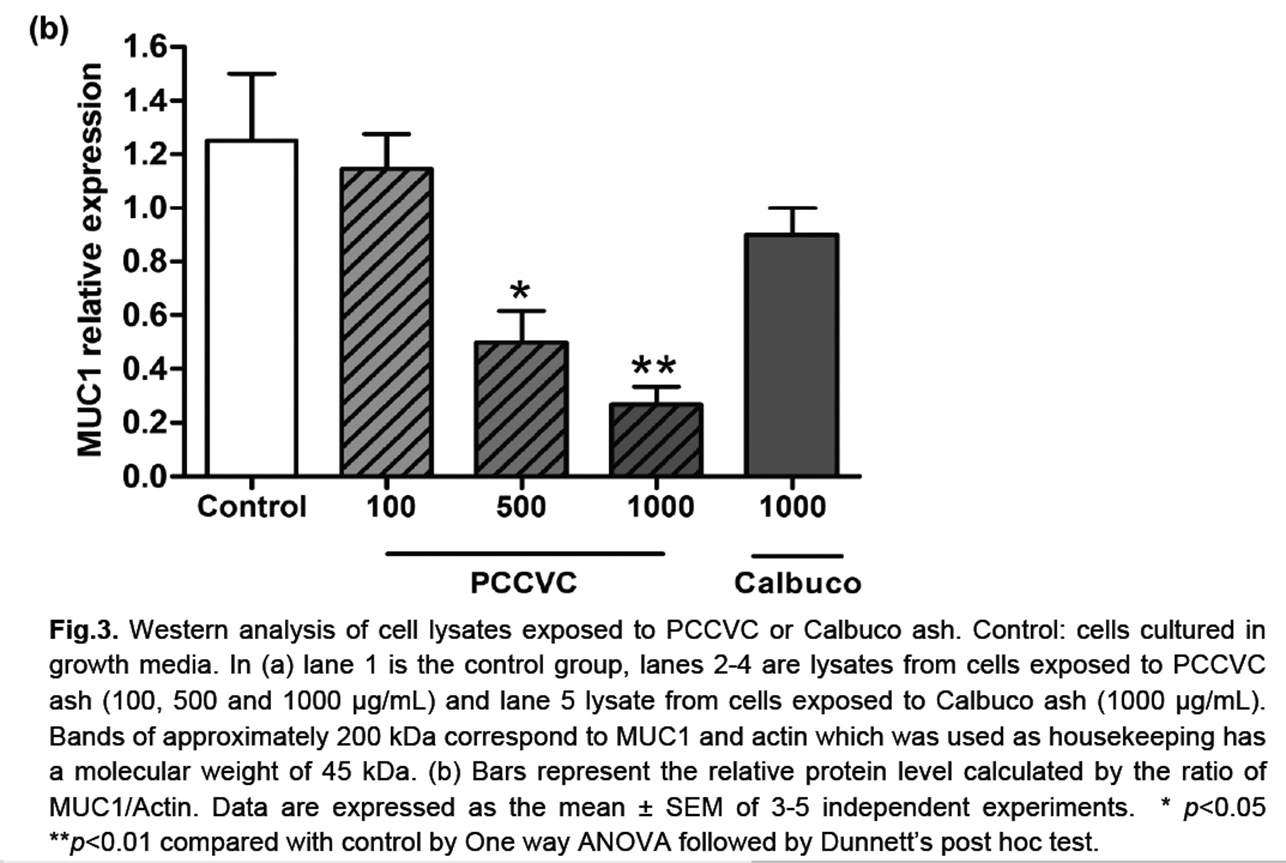
Figura 40: Western analysis of cell lysates exposed to PCCVC or Calbuco ash. Control: cells cultured in growth media. In (a) lane 1 is the control group, lanes 2-4 are lysates from cells exposed to PCCVC ash (100, 500 and 1000 µg/mL) and lane 5 lysate from cells exposed to Calbuco ash (1000 µg/mL).
Bands of approximately 200 kDa correspond to MUC1 and actin which was used as housekeeping has a molecular weight of 45 kDa. (b) Bars represent the relative protein level calculated by the ratio of MUC1/Actin. Data are expressed as the mean ± SEM of 3-5 independent experiments. * p<0.05
**p<0.01 compared with control by One way ANOVA followed by Dunnett’s post hoc test.
Las cenizas de los volcanes Puyehue y Calbuco indujeron la producción de ambas citoquinas proinflamatorias (IL-6 y IL-8) en las células de epitelio de conjuntiva normal. El aumento de ambas citoquinas fue mayor y significativo en las cenizas del Puyehue. Es importante destacar que la IL-8 es una citoquina con fuerte acción quimiotáctica de neutrófilos, con lo que ello significa.
El estudio de la producción de especies reactivas del oxígeno y del nitrógeno mostró que las cenizas del Puyehue, pero no las del Calbuco, estimulan dichas producciones en conjuntiva (Fig. 41).
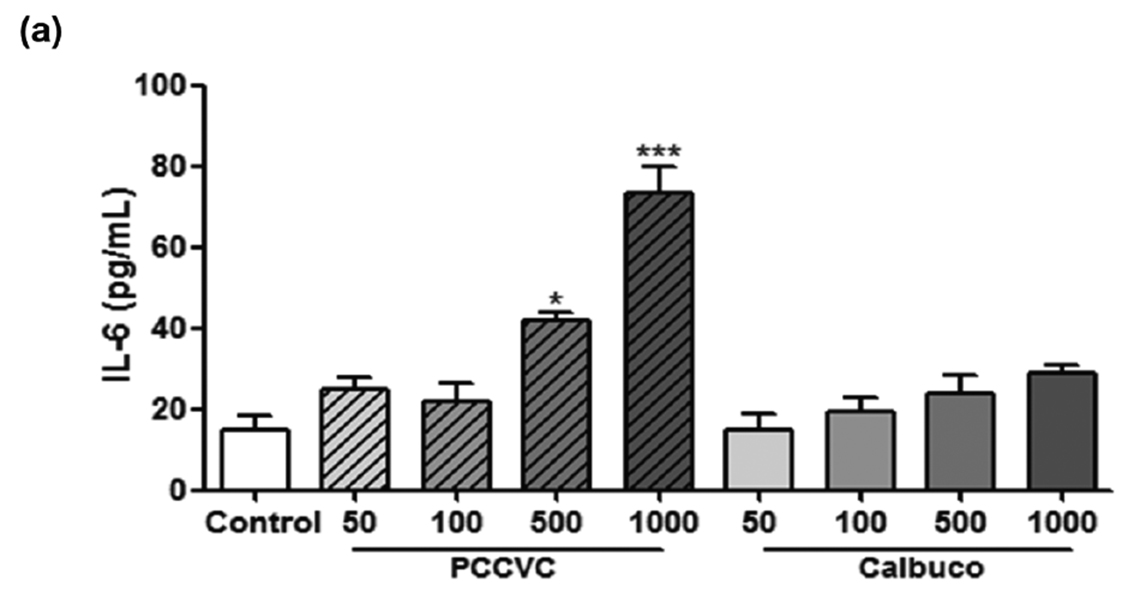
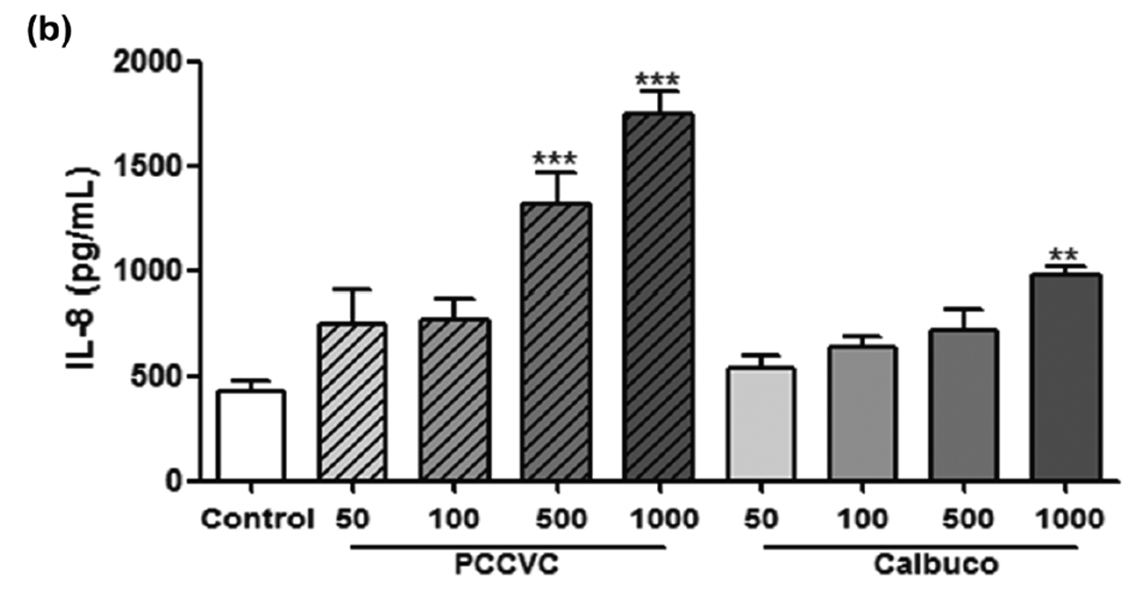
Figura 41: IL-6 (a) and IL-8 (b) released in supernatants of IOBA-NHC cells. Control: cells cultured in growth media. Results are mean values ± SEM of n=3-5 independent experiments. *P<0.05 **P<0.01 ***P<0,001 compared with control by ANOVA followed by Dunnett’s post hoc test.
Como sabemos, la contaminación del aire como el ojo seco afectan a cientos de millones de habitantes de centros urbanos 24. En ambos casos, la inflamación desempeña un rol crucial en las consecuencias deletéreas sobre la salud, constituyendo un problema que atañe a la salud pública.
Table 1. IOBA-NIHC viability and apoplosis percentages

Values are expressed as mean ± SEM. Results are mean values of three independent experiments.
EFECTO DE LA EXPOSICIÓN CRÓNICA A LA CONTAMINACIÓN AÉREA DE BUENOS AIRES
En megaciudades, áreas céntricas de intenso tránsito vehicular, se caracterizan por la probabilidad de alta ocurrencia de niveles elevados de MP, especialmente de MP2,5. En la actualidad, la investigación en el campo de las enfermedades ambientales se esfuerza en poner de manifiesto la relación entre las características de la exposición al MP propia de cada área y las alteraciones en la salud de los individuos que la habitan 25.
Estudios recientes muestran que los niveles de MP frecuentemente encontrados en ambientes urbanos impactan negativamente sobre el medioambiente y la salud poblacional 26. Si bien se conocen los efectos adversos que provoca el MP sobre la salud, la mayoría de estos estudios se han realizado en ciudades de los Estados Unidos y Europa 26, 27. Las conclusiones de estos trabajos pueden no ser válidas en el contexto de ciudades latinoamericanas, entre ellas Buenos Aires, ya que poseen características climáticas, geográficas y socioeconómicas considerablemente diferentes.
La mayor parte de la contaminación aérea del MP y gaseosa observada en la ciudad de Buenos Aires es de naturaleza primaria y está relacionada directamente con las emisiones vehiculares 28, 29. Previamente mostramos que el MP de la ciudad de Buenos Aires se caracteriza por presentar principalmente partículas finas y ultrafinas 28, consideradas por su relación tamaño/volumen las más nocivas para la salud.
Los niveles recomendados por el gobierno de la Ciudad Autónoma de Buenos Aires (CABA) se basan en el reporte de la Agencia de Protección Ambiental de los Estados Unidos (EPA) de 1998 que establecen que los niveles aéreos recomendados para MP10 deben ser menores a 150 µg/m3,30 sin embargo, la Organización Mundial de la Salud (WHO) en 2005 estableció guías que recomiendan niveles menores en el aire de 50 µg/m3 para MP10.
En este contexto, en 2017, los niveles máximos en 24h (70 µg/m ) cumplen con EPA-1998 pero no con los de WHO-2005, además, el valor máximo en 1h de MP10 de CABA (220 µg/m3) no cumplen ni EPA-1998 ni WHO-2005. El gobierno de CABA no mide PM 2,5 . En 2018, Greenpeace Argentina hizo un relevamiento de la calidad del aire de CABA, mostrando que valores promedio de PM 2,5 supera en un 85% de los casos el nivel guía de exposición crónica de la OMS fijado para PM2, 5, 32.
La hiperosmolaridad y la contaminación ambiental poseen similares vías inmunoinflamatorias, por lo tanto consideramos que los oftalmólogos sobre-diagnostican ojo seco, cuando en realidad los síntomas y signos y el cuadro inflamatorio es debido a la contaminación del aire. En realidad el término correcto a utilizar por los oftalmólogos que evalúan a pacientes con irritación ocular, sensación de arenilla, BUT menor a 7 segundos, coloraciones vitales leves (lisamina verde o rosa de bengala) y test de Schirmer mayor a 10 mm/5min. y que viven en megaciudades donde los niveles de contaminación exceden los niveles recomendados por las guías de la Organización Mundial de Salud debería ser conjuntivitis urbana.
Por su exposición directa, la superficie ocular (conjuntiva, limbo y córnea) es un blanco directo de la acción de la contaminación ambiental aérea, en especial el material particulado (MP) 18, 19, 33.
El MP desencadena especies reactivas del oxígeno (ROS) que generan estrés oxidativo, induciendo genes involucrados en las vías de señalización relacionadas con la inflamación como algunas citoquinas pro inflamatorias (TNF-α, IL-1, IL-6, IL-8, IL-17), moléculas de adhesión, receptores tirosina quinasa, MAPKs, JNKs, NF-KB, Stat-1 de citoquinas y moléculas de histocompatibilidad 15. Este proceso podría implicar daño en el tejido epitelial de la córnea, limbo y conjuntiva con incremento de citoquinas proinflamatorias y activación de células presentadoras de antígenos, principalmente macrófagos y células dendríticas.
EFECTO DE LA EXPOSICIÓN CRÓNICA DE LA CIUDAD DE SAO PAULO, BRASIL SOBRE LA SUPERFICIE OCULAR
Se evaluaron individuos normales expuestos a distintos niveles de contaminación aérea de São Paulo, Brasil. Los individuos recibieron un monitor individual de contaminación que estuvieron expuestos en zona expuesta por 7 días (Fig. 42). Luego los individuos se dividieron en 4 grupos según el nivel de exposición aérea individual. Utilizando medidores individuales de NO2 y citología de impresión conjuntival, nuestros resultados evidenciaron una asociación significativa entre el nivel de exposición a la contaminación de São Paulo e hiperplasia de células caliciformes, sugiriendo que la superficie ocular se adapta a la contaminación ambiental, produciendo mayor cantidad de células caliciformes con mayor producción de mucus aumentando de esta manera la interfaz entre el medio ambiente y la superficie ocular. En la figura se observa que cuanto mayor es el nivel de exposición mayor es la cantidad de células caliciformes que presenta voluntario sano en conjuntiva (Fig. 43).

Figura 42
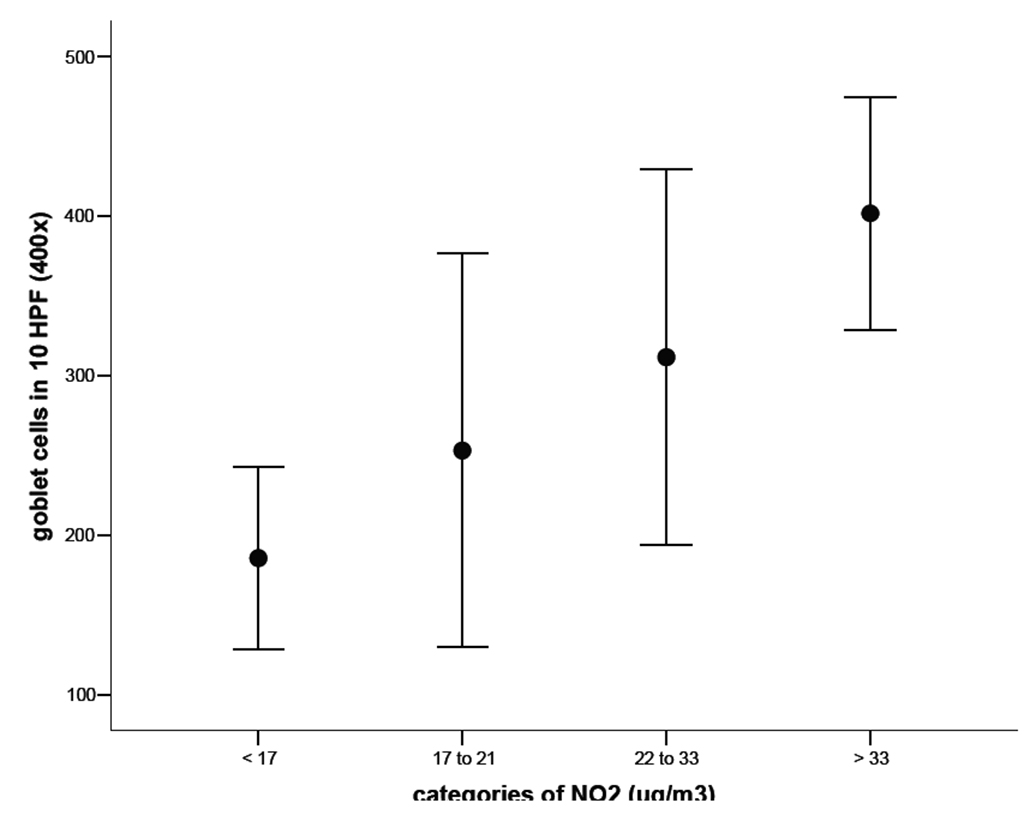
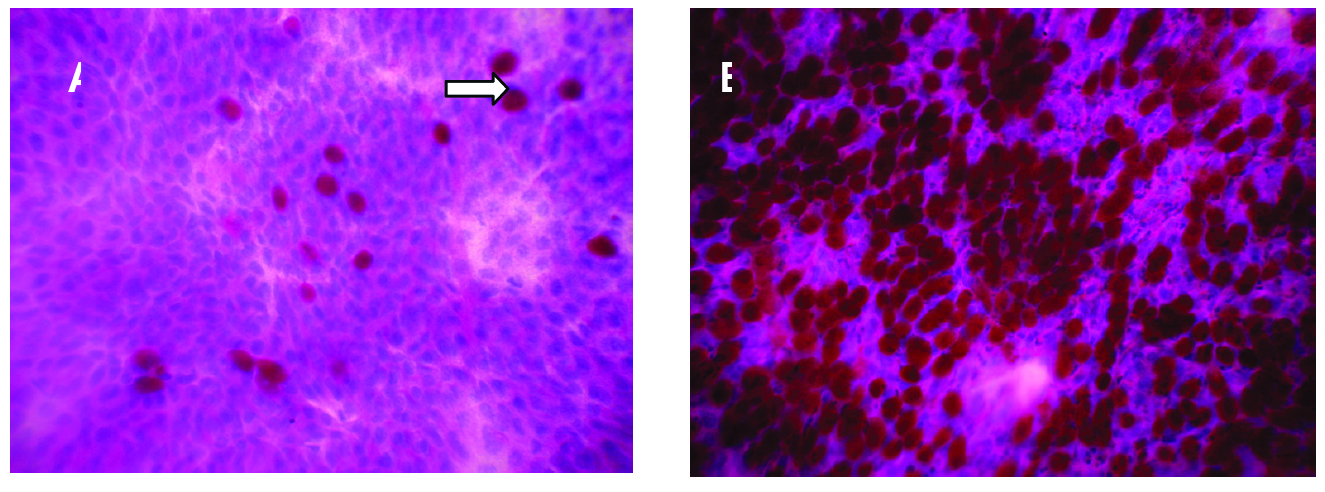
Figura 43
En las figuras se observan: el monitor y como va expuesto por 7 días, una citología de impresión en individuos pocos expuestos y muy expuestos y, los cantidad de células caliciformes y niveles de exposición aérea.
En otra serie de estudios evaluamos los síntomas y signos de 55 voluntarios expuestos a distintos niveles de exposición individual al aire de la ciudad de São Paulo, Brasil utilizando la misma metodología anterior.
Los niveles de exposición fueron divididos en 4 cuartiles
| Cuartil |
NO2 |
|
| (µg/ m3) |
Cantidad |
|
| de pacientes |
|
| 1 |
9.9 – 20.0 |
13 |
| 2 |
20.1 – 26.0 |
14 |
| 3 |
26.1 – 35.0 |
14 |
| 4 |
> 35.0 |
14 |
En el estudio por la encuesta OSDI evidenció una clara asociación exposición-síntomas, obviamente cuanto mayor era el nivel de exposición del voluntario mayor era el escore OSDI (p=0.01).
Además encontramos un claro patrón entre exposición-síntomas de irritación ocular (p <0,05) y la exposición-inestabilidad lagrimal (p <0.05, r = -0,316, correlación de Spearman) 19. Un dato interesante también encontrado fue que los voluntarios del cuartil 4 (> 35.0 µg/ m3 de NO2) tuvieron una asociación positiva con la presencia de meibomitis.
Estos estudios muestran que el OSDI si bien es una buena herramienta para los pacientes con ojo seco, tiene una asociación directa con los niveles de contaminación del aire. Este hecho puede confundir al oftalmólogo en el diagnóstico de certeza del ojo seco.
EFECTO DE LA CONTAMINACIÓN AÉREA DE BUENOS AIRES SOBRE LA SUPERFICIE OCULAR DE VOLUNTARIOS NORMALES
Se sabe que Buenos Aires representa la ciudad con mayor cantidad de habitantes de Argentina, en donde, habitan aproximadamente 3 millones de personas en 200 km2 de superficie. Si consideramos el área metropolitana de Buenos Aires (AMBA) constituida por la ciudad y 24 distritos del conurbano, esta cifra asciende a 15 millones de habitantes. Dado que existe una alta incidencia afecciones en la superficie ocular y las vías respiratorias en la población de AMBA, es posible que la contaminación aérea, a la que esta población está expuesta, presente un efecto deletéreo por si mismo y/o exacerbe enfermedades preestablecidas, por ejemplo, ojo seco.
En la Ciudad de Buenos Aires existe una red de monitoreo de calidad de aire y ruido (Agencia de Protección Ambiental, GCBA).
Se miden actualmente en tres Estaciones de Monitoreo Atmosférico, ubicadas respectivamente en Av. Córdoba y Callao, La Boca y en Parque Centenario, todas ellas pertenecientes a la Dirección General Control de Calidad Ambiental del Gobierno de la Ciudad de Buenos Aires34. Son automáticas y continuas, de modo que funcionan en forma permanente.
Es conocido que el tipo de contaminación aérea de cada ciudad depende de la cantidad y tipo de vehículos (motores diesel, nafteros, eléctricos, mixtos), industrias, geografía, etc. Por lo tanto, los datos obtenidos en una ciudad no necesariamente son asimilables a otras.
EVALUACIÓN DE PARTÍCULAS EMITIDAS POR MOTORES DIESEL DE SAO PAULO, BRASIL Y BUENOS AIRES, ARGENTINA
En nuestro caso, comparamos las partículas emitidas por motores diesel (DEP) (Fig. 44). Cabe destacar que los motores diesel en Brasil y Argentina son similares y que los resultados en el análisis del espectro atómico y la evaluación por microscopía electrónica fue también similar.
Nosotros encontramos que el DEP puede ser endocitado por las células epiteliales de la conjuntiva humana. En la figura 45 se observa dicho fenómeno.

Figura 44: Imágenes representativas de las DEP obtenidas en el microscopio electrónico de transmisión. Se pueden apreciar los agregados (A) que forman las partículas prácticamente esféricas (B) y sus tamaños (C). Aumentos: A = 7000x, B = 85000x, C = 140000x
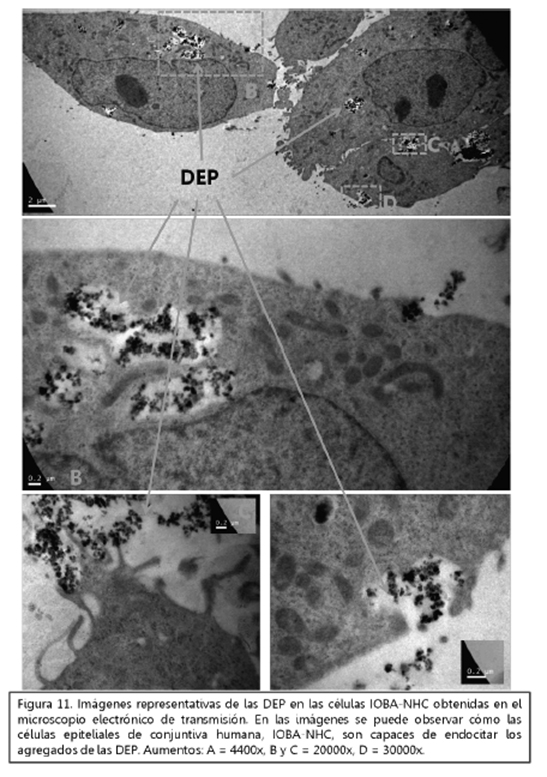
Figura 45: Imágenes representativas de las DEP en las células IOBA-NHC obtenidas en el microscopio electrónico de transmisión. En las imágenes se puede observar cómo las células epiteliales de conjuntiva humana, IOBA-NHC son capaces de endocitar los agregados de las DEP. Aumentos: A = 4400x, B y C = 20000x, D = 30000x.
En las células conjuntiva humana con DEP100 se visualizaron con claridad los agregados electrodensos de las DEP dentro de las células en vesículas citoplasmáticas tipo fagosomas (Figura. 10 y 11 A-B). Se observaron protrusiones de la membrana plasmática tipo seudópodos interaccionando con las DEP, lo que indicaría que estas protrusiones estarían involucradas en la captación de DEP hacia el interior celular. Es decir, las células epiteliales de conjuntiva, son capaces de endocitar las DEP por un mecanismo tipo fagocitosis.
El estudio del material particulado (MP-BA) de Buenos Aires mostró diferencias en su composición atómica de acuerdo a la época del año estudiada (Figs. 46 A y B).
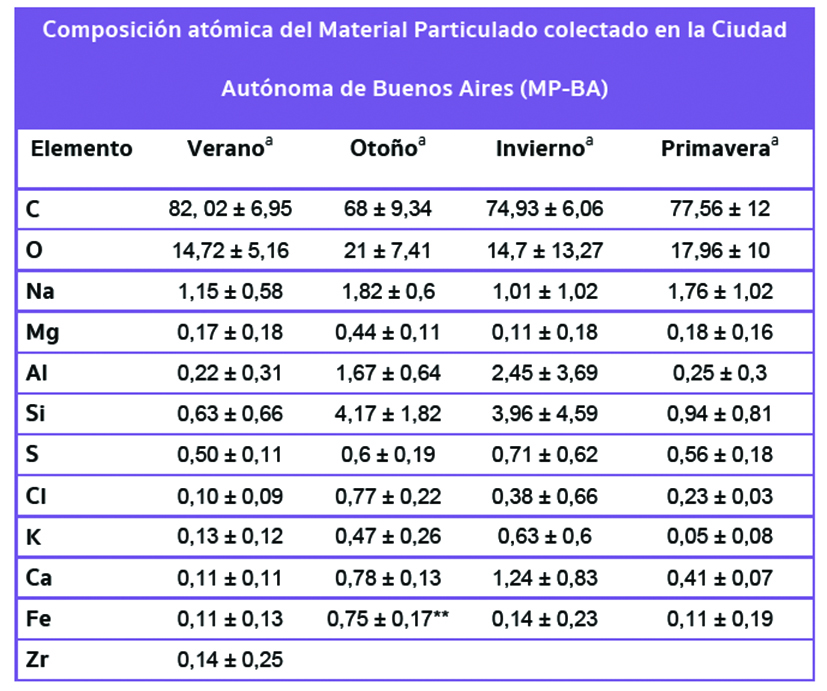
Figura 46 A

Figura 46 B: Imágenes representativas del PM-CABA obtenidas en el microscopio electrónico de barrido. Se pueden apreciar los agregados (A) que forman las partículas prácticamente esféricas y sus tamaños (B). Aumentos A = 50000x, B = 200000x.

*Porcentaje expresado como media ± desvío estándar.
EFECTO DEL MATERIAL PARTICULADO DE BUENOS AIRES SOBRE ÚLCERAS CORNEALES Y HERIDAS
Las células de conjuntiva humana mostraron una disminución en la migración dosis dependiente al incubarlas con las DEP por 24 hs. Estas
disminuciones en los porcentajes de migración fueron significativas para las concentraciones de
50, 100 y 500 µg/mL de las DEP al compararlas con las células control (31%, p<0,01; 44%, p<0,01 y 81%, p<0,001, respectivamente) (Fig. 47). En la figura 48 se muestran los resultados obtenidos.
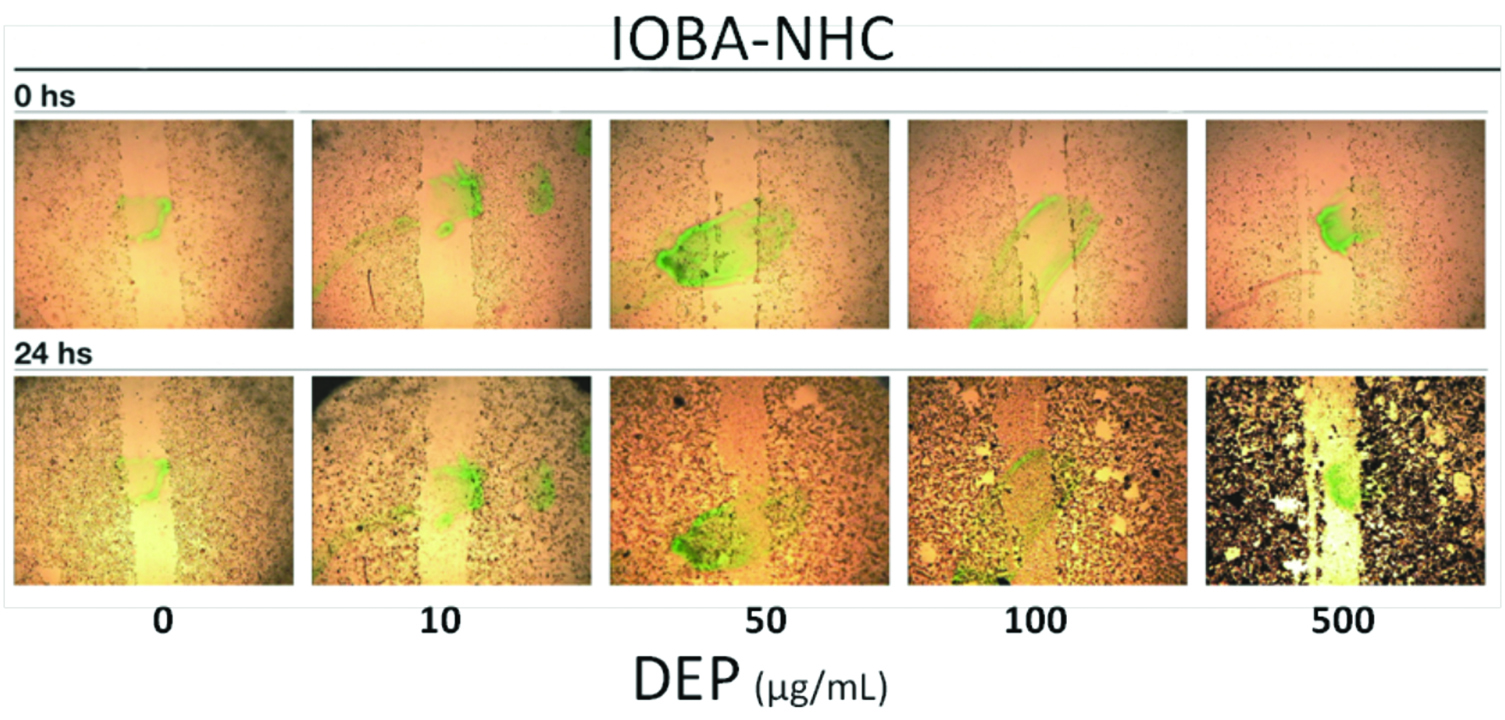
Figura 47
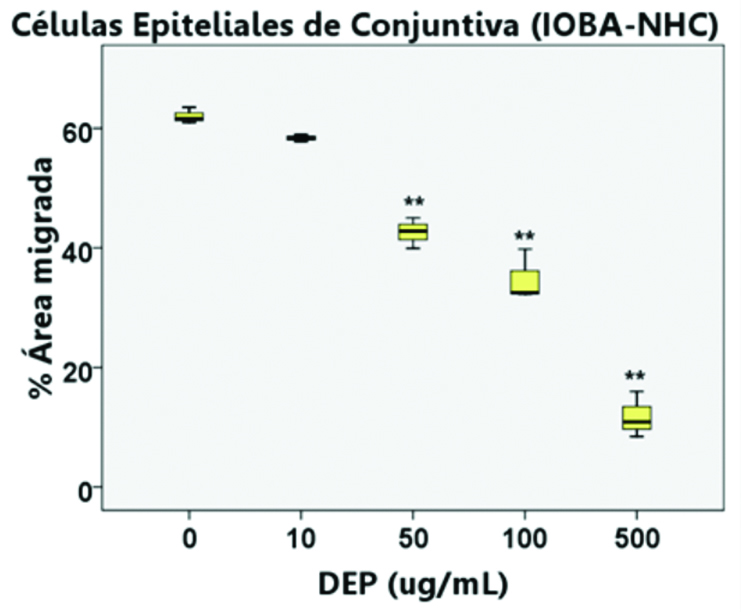
Figura 48 Ensayo de migración. A modo ilustrativo, se muestran imágenes representativas de las células IOBA-NHC a 400x de cada condición luego de haberse realizado la herida (tiempo 0, fila superior) y la misma zona de cada condición luego de incubarlas con las diferentes concentraciones de las DEP por 24hs. (fila inferior). El gráfico muestra los porcentajes migrados para cada condición **p.<0,01 versus control.
El estudio de la úlceras corneales en cultivos celulares y en ratones mostró que en los ratones expuestos a la contaminación aérea de Buenos Aires (UAP-BA) y DEP, las úlceras de córnea tardaban más en cicatrizar (Fig. 49).
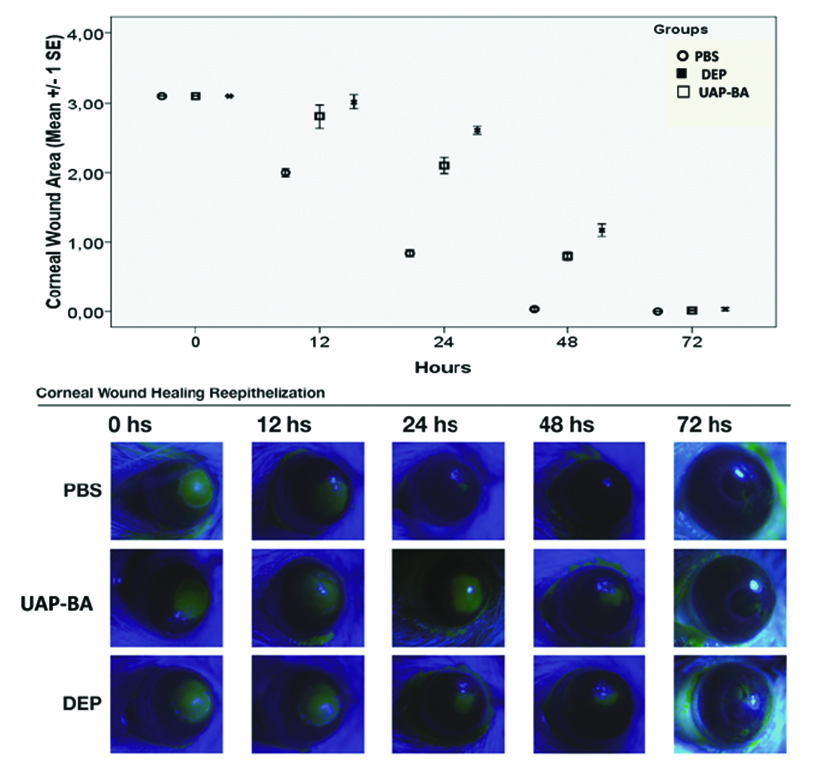
Figura 49
EFECTO DE LA CONTAMINACIÓN AÉREA DE BUENOS AIRES SOBRE LA SUPERFICIE OCULAR DE PACIENTES CON SÍNDROME DE SJOGREN
Para evaluar si la contaminación ambiental exacerba los síntomas y signos de ojo seco, conjuntamente con el Dr. Gustavo Galperin evaluamos la superficie ocular con ojo severo por Síndrome de Sjögren. Utilizamos monitores individuales de contaminación. Tanto los pacientes con Síndrome de Sjögren como los voluntarios sanos portaron los monitores en zona expuesta por una semana. De esta manera pudimos determinar los niveles de exposición de cada individuo.
| Variables |
|
|
| Media ± DE |
|
|
| (Min - Max) |
Pacientes |
|
| (n= 30) |
Familiares |
|
| (n = 30) |
|
|
| Cuestionario OSDI |
2,57 ± 0,84 (1 - 4) |
0,95 ± 0,75 |
| (0 - 2) |
|
|
| Test de Schirmer I |
4,95 ± 2,25 (1 - 11) |
13,70 ± 1,39 |
| (11,5 - 17) |
|
|
| TBUT |
3,97± 1,47 |
|
| (2 - 7) |
7,25 ± 1,9 |
|
| (5 - 12) |
|
|
| Test de Lisamina Verde |
3,04 ± 2,04 |
|
| (1 - 6) |
0,30 ± 0,46 |
|
| (0 - 1) |
|
|
| Test de |
|
|
| Fluoresceína |
2,34 ± 1,35 |
|
| (0 -4) |
0,2 ± 0,62 |
|
| (0 - 1) |
|
|
| Citología de |
|
| Impresión |
1,89 ± 0,92 |
|
| (0 - 3) |
0,45 ± 0,44 |
|
| (0 - 1,5) |
|
|
| Lisozima |
|
|
| Lagrimal |
751,25 ± 244,73 (350 - 1500) |
1409,90 ± 188,21 (1050 - 1750) |
| Dosaje de NO2 |
29,20 ± 12, 1 |
|
| (11,1 - 57,8) |
28,21 ± 11,70 |
| (12,1 - 49,5) |
|
|
Según el nivel de exposición todos los individuos fueron divididos en tres cuartiles, exposición baja (verde) exposición moderada (beige) y exposición alta (azul).
OSDI
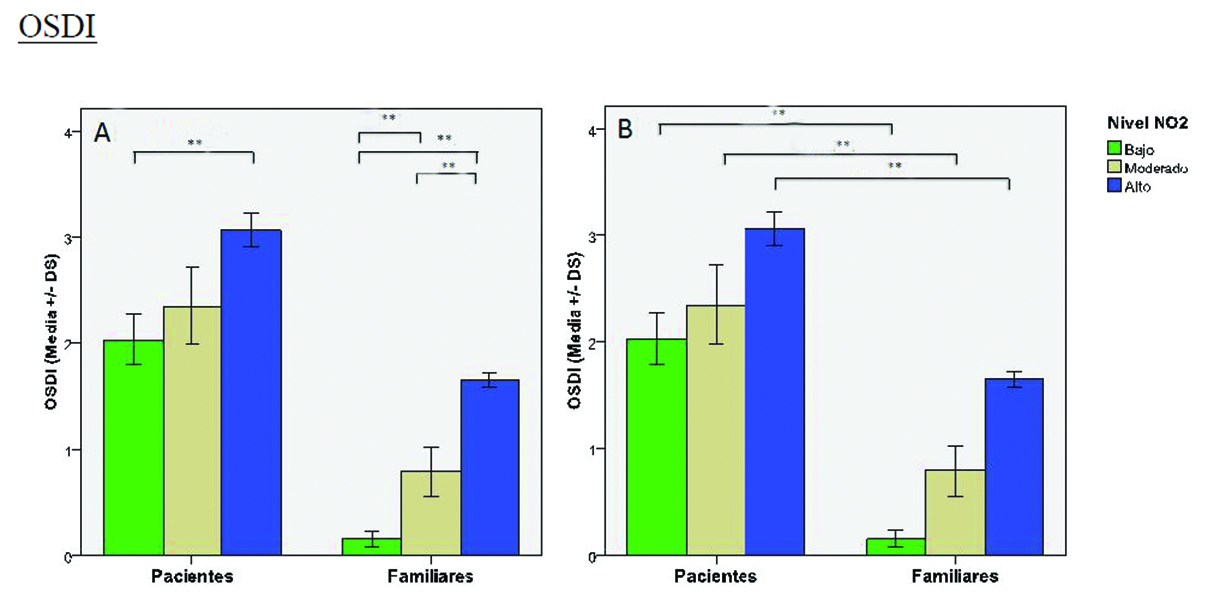
En (A) se observa que sólo es significativa la diferencia entre pacientes de baja versus alta exposición (p< 0.001); En el grupo de familiares se encontraron diferencias significativas (p< 0.001) entre entre todos los grupos entre sí.
En (B) se evidencia intergrupos que ante similar nivel de exposición, los pacientes presentan mayor escore de síntomas según la encuesta OSDI que los familiares (p< 0.001).
Tiempo de ruptura de la película lagrimal (BUT)

En (A) se observa entre pacientes diferencias significativas entre niveles bajos respecto al altos de exposición (p< 0.001). En el grupo de familiares se encontraron diferencias significativas entre baja versus moderada exposición (p< 0.005); baja versus alta exposición (p< 0.001) y moderada versus alta exposición (p<0.001). La inestabilidad del film lagrimal evaluada por el BUT resultó ser más sensible en familiares que en pacientes con distintos niveles de exposición.
En (B) se evidencia estadísticamente (p< 0.001) que similar nivel de exposición, los pacientes presentan menor estabilidad de la película lagrimal según el BUT.
* significa p<0.005 ;** significa p< 0.001
Lisamina de verde
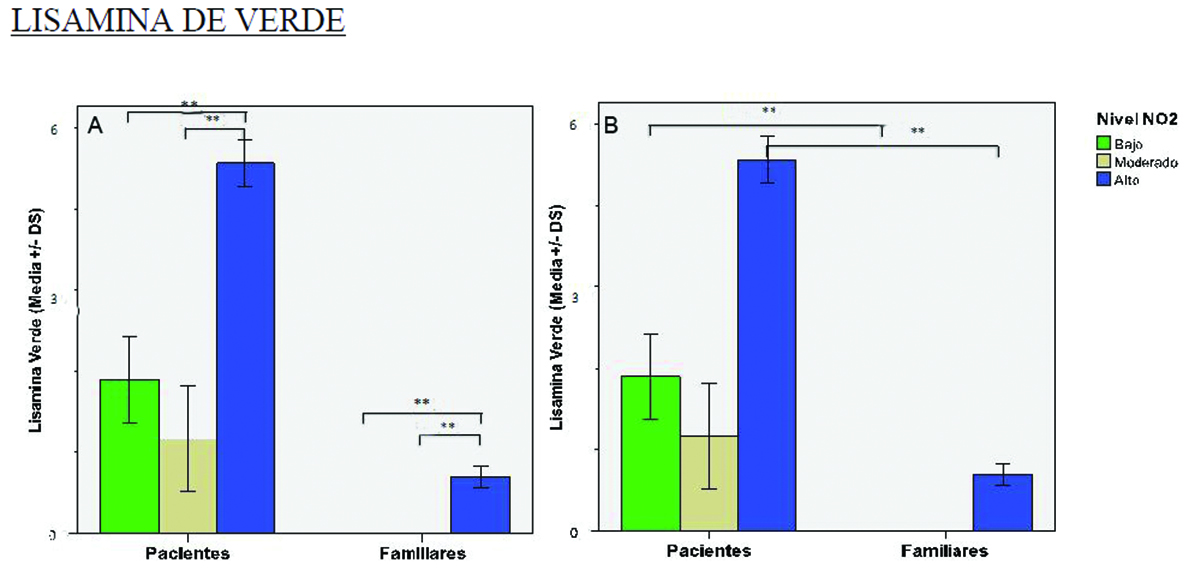
En (A) se observa entre pacientes diferencias significativas entre niveles bajos respecto al altos de exposición (p< 0.001) y medios respecto a altos (p< 0.001). En el grupo de familiares se encontraron diferencias significativas entre baja versus alta exposición(p< 0.001) y moderada versus alta exposición (p< 0.001). Los resultados expresados en estos gráficos expresan claramente la relación directa entre el nivel de exposición a NO2 y el daño de la superficie ocular.
En (B) se evidencia estadísticamente (p< 0.001) para bajos nivel de exposición y para altos niveles de exposición.
** significa p< 0.001
Tinción con fluoresceína
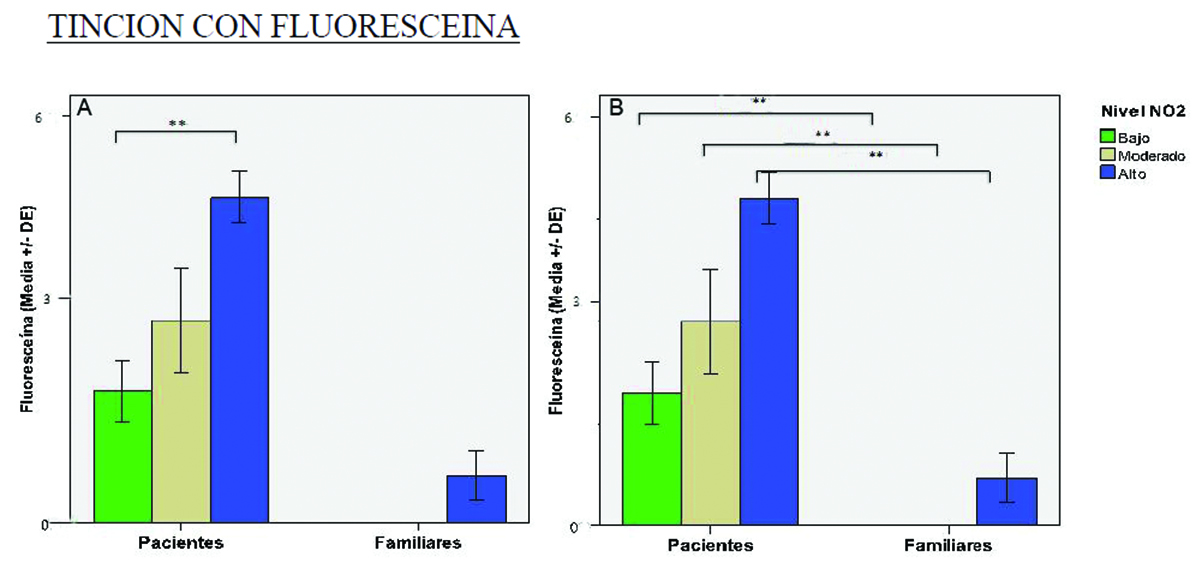
En (A) se observa entre pacientes diferencias significativas entre niveles bajos respecto al altos de
exposición (p< 0.001). En el grupo de familiares no se encontraron diferencias significativas. Se observa que en los pacientes el daño del epitelio corneal se correlaciona directamente con el grado de exposición.
En (B) se evidencia que para similares niveles de exposición el daño del epitelio corneal es significativo (p< 0.001).
** significa p< 0.001.
| Test |
|
|
|
| Oftalmológicos |
Nivel de |
|
|
| Exposición |
Test Estadísticos (α= 0,05) |
|
|
ANOVA (p) |
Bonferroni (p) |
| OSDI |
Alta vs Baja |
0.001 |
< 0.001 |
| BUT |
Alta vs Baja |
0.001 |
< 0.001 |
| Verde de Lisamina |
Alta vs Baja |
< 0.001 |
< 0.001 |
|
Alta vs |
|
|
| Moderada |
< 0.001 |
< 0.001 |
|
| Tinción |
|
|
|
| Corneal con Fluoresceína |
Alta vs Baja |
< 0.001 |
< 0.001 |
| Citología de Impresión Conjuntival |
Alta vs |
|
|
| Baja |
< 0.001 |
< 0.001 |
|
|
Alta vs |
|
|
| Moderada |
< 0.001 |
< 0.001 |
|
Nuestros resultados muestran que en el grupo de pacientes con ojo seco severo, la exposición a mayores niveles de contaminación (NO2), produjo afectación estadísticamente significativa en los siguientes tests: OSDI, BUT, lisamina verde, tinción corneal con fluoresceína y citología de Impresión conjuntival. Estos cambios fueron más evidentes en los grupos de alta exposición. Se verificaron cambios significativos en los pacientes con una exposición moderada solo en la tinción con verde de lisamina y citología de impresión conjuntival.
El análisis de familiares de pacientes mostró que niveles altos de exposición produce síntomas de malestar ocular (encuesta OSDI), inestabilidad del film lagrimal (BUT) y alteraciones en las células conjuntivales (citologia de impresión).
El análisis por niveles de exposición intergrupo (pacientes versus familiares) evidenció cambios significativos en todos los parámetros evaluados (OSDI, Schimer, BUT, lisamina verde, fluoresceína, citología de impresión y lisozima).
PARTICIPACIÓN DE LOS MACRÓFOGOS EN LA SUPERFICIE OCULAR AFECTADA POR LA HIPEROSMOLARIDAD Y CONTAMINACIÓN AÉREA
Los macrófagos (Mφ) por su capacidad de capturar, procesar y posteriormente presentar antígenos orquestan, la respuesta inmune y desempeñan un papel central en la patogénesis de muchos trastornos mediados por el sistema inmunoinflamatorio.
Previamente, mostramos que la presencia a partículas emitidas por motores diesel (DEP) provoca alteraciones similares a las observadas en la enfermedad del ojo seco35, 36 induciendo apoptosis en células epiteliales y liberación de la citoquina proinflamatoria IL-637.
En los Estados Unidos, la gran prevalencia del ojo seco tiene una carga económica de $ 3.800 millones en gastos anuales de atención médica y de productividad reducida y, costos indirectos asociados con esta condición crónica a aproximadamente $ 55.000 millones1. En nuestro país, la prevalencia, incidencia y gastos en salud aún no han sido estimados, empero, es sabido que es la segunda causa de consulta oftalmológica luego de la prescripción de lentes y, que la venta de lubricantes oculares (lágrimas artificiales) y fármacos para el tratamiento de ojo seco es la franja terapéutica que más creció en últimos diez años en el
mercado oftalmológico.
El informe Dry Eye Workshop II de la International Society of Tear Film and Ocular Surface (TFOS DEWS II 2017) elaborado por más de 150 representantes de sociedades científicas y universidades de 23 países centra a la hiperosmolaridad en el comienzo de la inflamación del ojo seco. La hiperosmolaridad activa las vías de MAPk y NF-κB que inducen la producción diversas citoquinas proinflamatorias (IL-1ß, IL-6, IL-17, IFN-γ, TNF-α)11. En este contexto, células presentadoras de antígenos, entre ellas los macrófagos (Mφ) residentes en la superficie ocular son activadas aumentando la expresión de CCR7 y MHC clase II 38 migrando al nódulo linfático adyacente al ojo y activando células T “naive” para diferenciarse en células T efectoras como Th17 (secretan IL-17) y Th1 (secretan IFN-γ) por sobre células T regulatorias (Treg) 39. La respuesta Th17 está asociada al defecto en la barrera epitelial y al desarrollo de respuesta inmuno-inflamatoria, típica de la enfermedad del ojo seco39, 40.
Como se mencionó anteriormente, el MP desencadena la generación de especies reactivas del oxígeno (ROS) que provocan estrés oxidativo en líneas celulares de epitelio humano normal de córnea y conjuntiva, induciendo la activación en las vías de señalización relacionadas con la inflamación como algunas citoquinas proinflamatorias y MAPKs, JNKs, NF-kB 15, 41, 42. Este proceso podría implicar alteraciones funcionales en el tejido epitelial de la córnea y la conjuntiva con incremento de citoquinas proinflamatorias y polarización de Mφ.
Actualmente se considera que el MP de megaciudades puede inducir procesos inflamatorios sobre las mucosas de manera directa y/o exacerbar patologías preestablecidas.
Los Mφ son células heterogéneas y versátiles que muestran una notable plasticidad fenotípica y diversidad funcional 43, 44, 45. Por lo tanto, los Mφ activados a menudo se clasifican según su polarización en: fenotipo activado de forma clásica (M1) y fenotipo activado alternativamente (M2) 44, 45. Los Mφ-M1 son inducidos por IFN-γ o estímulos microbianos (LPS) y se caracterizan por la expresión de altos niveles de iNOS 46, 47. Después de la activación, los Mφ-M1 secretan citoquinas proinflamatorias (IL-1ß, TNF-α, IL-12 e IL-23) y quimioquinas (CXCL9 y CXCL10) e inducen inflamación y destrucción tisular 48. Por el contrario, los Mφ-M2 se polarizan por IL-4, IL-13 y glucocorticoides y se caracterizan por una alta expresión de receptor de manosa (CD206) y producción de IL-10, una citoquina antiinflamatoria que resuelve la inflamación y promueve la curación de heridas 48. Soc-1 actúa en la polarización de Mφ-M2 induciendo la producción de Arginasa y disminuyendo iNOS 49.
La polarización de Mφ-M1/M2 fue encontrada en la fase crónica de numerosas y diversas patologías, entre ellas, fibrosis, curación de heridas, dermatitis atópica, granuloma, diabetes, aterosclerosis, artritis, lupus, infecciones virales, etc.50, 51.
En la superficie ocular, You et al. 52 demostraron que después de someter a los ratones C57BL/6 al estrés de desecación, aumentaron la producción de marcadores de Mφ-M1 conjuntamente con la expresión de las citoquinas inflamatorias IL-18 e IL-12 producidas por los Mφ-M1 activados en la conjuntiva 52. Lee et al. 53, utilizando el mismo modelo experimental murino de ojo seco encontró un aumento en la polarización de Mφ-M1 con disminución de Mφ-M2.
Comprender los mecanismos de polarización de los Mφ y la modulación de sus fenotipos podría proporcionar una gran perspectiva para el diseño de nuevas estrategias terapéuticas.
Es sabido que los glucocorticoides intervienen en la polarización de los Mφ-M254 y resultan sumamente efectivos para el tratamiento del ojo seco, pero los efectos adversos como el aumento de la presión ocular y el desarrollo de catarata hace que su uso se vea limitado a cortos períodos de tiempo50. La investigación traslacional es necesaria para seguir desarrollando estos y otros enfoques innovadores a la vez que se minimizan los efectos adversos.
Hasta el momento la administración de drogas y alimentos de los Estados Unidos (FDA) sólo ha aprobado dos medicamentos para el tratamiento del ojo seco: emulsión oftálmica de ciclosporina al 0,05% (Restasis, Allergan) y una solución oftálmica que actúa como antagonista de antígeno 1 asociados a la función de los linfocitos (LFA-1) 0,5% (Xiidra, Shire). En algunos países como Japón, se comercializan más medicamentos para el tratamiento de la enfermedad ocular seca que en los Estados Unidos dado que las normas de aprobación no son tan rigurosas 55. Existen varios fármacos que se encuentran en fase III, entre ellos fosfato de dexametasona, Rimexolona, Bromfenac, inhibidores de receptores de citoquinas; inhibidores de la activación de células T y secretagogos de mucinas55. Otro factor importante relacionado con el tratamiento de la enfermedad del ojo seco es que, en la mayoría de los casos, las compañías de biotecnología intentan resolver el problema aliviando los síntomas en lugar de llegar a develar las causas de la enfermedad.
REPOLARIZACIÓN DE MACRÓFOGOS
Un tema de interés es estudiar la repolarización a Mφ-M2 como una nueva estrategia terapéutica. Una posibilidad puede ser mediante el tratamiento con Membrana Amniótica Humana liofilizada, micronizada, estéril (hAM-pe).
La Membrana Amniótica (MA) constituye la túnica más interna de la placenta56. En los últimos 100 años numerosos trabajos científicos han mostrado evidencias sobre las propiedades anticicatrizantes, antiinflamatorias, antifibróticas y antiangiogénicas de la MA 57, 58, 59. En el adulto la reparación de las heridas va acompañada por inflamación y cicatrices, que implican fibrosis e infiltrados celulares de neutrófilos, Mφ y linfocitos. En contraste con lo que pasa en el adulto, la reparación en una herida fetal está característicamente conocida como “sin cicatrices” 60, 61. Es sabido que luego de un lesión en el embrión, la respuesta inflamatoria es menos marcada y difiere en función de los tipos y número de células inflamatorias que participan en la reparación 62 y disminución de IL-8 e IL-6 63, 64.
Se ha demostrado que el MA humana puede inducir apoptosis 65, 66, disminución de factores secretados por Mφ-M1 (TNF-α, IL-6, CD68 y MHC II) y el aumento de factores secretados por los Mφ-M2 (IL-10) 66. Ambas respuestas pueden ser reguladas por una disminución de células T reguladoras (Treg) que activan Mφ-M2 67.
Hasta el momento, el uso de la MA es estrictamente quirúrgico y está ampliamente extendido en tratamiento de úlceras dérmicas y oftalmológicas y en procesos de neovascularización de la córnea causantes de ceguera, pudiendo convertirse en una eficaz alternativa terapéutica en patologías inflamatorias, neovasculares, y cicatrizales tanto de la piel como de la córnea 68, 69, 70, 71.
Se ha demostrado que la expresión de TGF-ß está disminuida en fibroblastos corneales y conjuntivales humanos cultivados sobre MA 59, 72. Además, la MA trasplantada en la superficie de la córnea también muestra una reducción de vascularización 73. El efecto antiangiogénico de la MA se utiliza actualmente para la reconstrucción de la superficie de la córnea y en el trasplante de células madre epiteliales de la del limbo corneal 74, 75, 76La MA puede polarizar a Mφ-M2 luego de su unión TLR 77.
La utilización como extracto o pulverizado ha sido muy poco estudiado. Se ha encontrado que el extracto de MA 78 previene la angiogénesis corneal e inhibe en forma dosis-dependiente la viabilidad, proliferación y migración de neovasos corneales 79. Factores secretados por MA pulverizada impactan en la repolarización de Mφ-1 a Mφ-M2 80.
Prevemos que la hAM-pe podrá utilizarse como una nueva plataforma de lanzamiento de agentes terapéuticos que permitan ayudar a la medicina regenerativa y la polarización de Mφ en el futuro 80.
AGRADECIMIENTOS
Estos trabajos realizados durante los últimos diez años no podrían haber sido realizados sin el esfuerzo y dedicación de los Dres. Julia Tau, Alejandro Aguilar, Martin Berra, Gustavo Galperin, Cristina Aguado, Pablo Gruccio, Patricio González Valdes, Pablo Chiaradia, Silvana Albornoz, Felipe Gutiérrez, Newton Kara jose, Priscila Novaes y el apoyo económico de las universidades de Buenos Aires y São Paulo y, del Ministerio de Ciencia y Técnica de Argentina.
BIBLIOGRAFÍA
1. Hirschberg, J. The history of Ophthalmology. I Antiquity. (1899), p 73.
2. Voinot, J. Inventaire des cachets d´oculistes gallo-romains. Conf Lyon. Ophthalmol. (1981).
3. Wenzel, M. Manuel de l´oculiste ou dictionnaire ophthalmologique. Paris: Boureau du Lavater (1808). 2v.
4. Mackenzie, W. Xeroma conjunctival ou xérophthalmie. Traté des maladies de l´oeil. Paris: Masson (1856).
5. Schirmer, O. Studien zur Physiologie und Pathologie der Tränenabsonderung un Tränenabfluss. Graefe´s Aech. Ophthalmol. 56 (1903): 197.
6. Gourgerot, M. Insuffisance progresive et atrophie des glandes salivaires et muqueuses de la bouche, des conjunctives. Bull. Soc. Fr. Derm. Syph. 25 (1925): 376-379.
7. Sjögren, H. Zur kenntnis der keratoconjunctivitis sicca. Acta Ophthalmol (Kbh). (1933): 1-151.
8. Balik, J. The lacrimal fluid in keratoconjunctivitis sicca. Am J. Ophthalmol. (1952): 773-781.
9. Mishima, S. Some physiological aspects of the precorneal tear film. Arch. Ophthalmol. (1965): 233-241.
10. Ehlers, N. The precorneal film. Acta Ophthalmol (Kbh). (1965).
11. Brown, S.I.; Mishima, S. The effect of blinking on tear concentrationand corneal hydration. Invest. Ophthalmol (1965): 946.
12. Norm, M.S. Dessication of the precorneal film. Corneal wetting time. Acta Ophthalmol. (1969): 865-880.
13. Van Bijterveld, O.P. Diagnostic tests in the sicca síndrome. Arch. Ophthalmol. (1969): 10-14.
14. Holly, F.J.; Lemp, M. Wetability and wetting of corneal epithelium. Exp. Eye. Res. (1971): 239-250.
15. Aguilar, A.J.; Rodriguez, M.; Fonseca, L.; Marré, D. El test de Schirmer como método de medida de la concentración de sodio del film lagrimal y de su osmolaridad en pacientes portadores de ojo seco. Claves de la fisopatología de la lesión sicca. Arch. Oftal. De Bs. As. (1993), 68: 189-193.
16. Aguilar, A. J.: Ojo seco, manual sobre fisiopatogenia, diagnóstico y tratamiento. Ediciones Científicas Argentinas. Buenos Aires. 1999. 193p.
17. Berra A, Berra M. Hyperosmolarity induce nuclear translocation of NF-B in human conjunctiva epithelial cells. Invest Ophthalmol Vis Sci. (2005): 46.
18. Lemp, M. Report of the National Eye Institute/ Industry Dry Eye Workshop. CLAO Journal. (1995): 221-232.
19. Foulks, G.; et al.International Dry Eye Workshop (DEWS). (2007).
20. Geerling. G., Baudouin C., et al. Emerging strategies for the diagnosis and treatment of meibomian gland dysfunction. Proceedings of the Ocean group meeting. The Ocular Surface (2017).
21. Berra, I.; Aguilar, A.J.; Berra. A. Clinical and laboratory tests in patients with dry eye, allergic conjunctivitis and dry eye plus allergic conjunctivitis. ARVO abstract (1999). Fort Lauderdale, Florida, USA.
22. Aguilar, A.J.; Fonseca, L.; Croxatto, J.O. Sjögren´s Syndrome: a comparative study of impression cytology of the conjunctiva and buccal mucosa, and salivary glang biopsy. Cornea (1991), 3: 203-206.
23. Yu, J., Asche, C.V. & Fairchild, C.J. The economic burden of dry eye disease in the United States: a decision tree analysis. Cornea 30, 379-387 (2011).
24. Schaumberg, D.A., Dana, R., Buring, J.E. & Sullivan, D.A. Prevalence of dry eye disease among US men:
estimates from the Physicians’ Health Studies. Arch Ophthalmol 127, 763-768 (2009).
25. Schaumberg, D.A., Sullivan, D.A., Buring, J.E. & Dana, M.R. Prevalence of dry eye syndrome among US
women. Am J Ophthalmol 136, 318-326 (2003).
26. Gilbard, J.P., Rossi, S.R., Gray, K.L., Hanninen, L.A. & Kenyon, K.R. Tear film osmolarity and ocular surface disease in two rabbit models for keratoconjunctivitis sicca. Invest Ophthalmol Vis Sci 29, 374-378 (1988).
27. Gilbard, J.P. & Farris, R.L. Tear osmolarity and ocular surface disease in keratoconjunctivitis sicca. Arch
Ophthalmol 97, 1642-1646 (1979).
28. Hagan, S. & Tomlinson, A. Tear fluid biomarker profiling: a review of multiplex bead analysis. Ocul Surf 11,
219-235 (2013).
29. Luo, L., Li, D.Q. & Pflugfelder, S.C. Hyperosmolarity-induced apoptosis in human corneal epithelial cells is mediated by cytochrome c and MAPK pathways. Cornea 26, 452-460 (2007).
30. Luo, L., Li, D.Q., Corrales, R.M. & Pflugfelder, S.C. Hyperosmolar saline is a proinflammatory stress on the mouse ocular surface. Eye Contact Lens 31, 186-193 (2005).
31. Pflugfelder, S.C. et al. Stress-activated protein kinase signaling pathways in dry eye and ocular surface disease. Ocul Surf 3, S154-157 (2005).
32. Craig, J.P. et al. The TFOS Dry Eye Workshop II: Executive Summary. Ocul Surf (2017).
33. Bron, A.J. et al. TFOS DEWS II pathophysiology report. Ocul Surf 15, 438-510 (2017).
34. Bell, M.L. et al. Environmental health indicators and a case study of air pollution in Latin American cities.
Environmental research 111, 57-66 (2011).
35. Bell, M.L., Davis, D.L., Gouveia, N., Borja-Aburto, V.H. & Cifuentes, L.A. The avoidable health effects of air pollution in three Latin American cities: Santiago, Sao Paulo, and Mexico City. Environmental research 100, 431-440 (2006).
36. United Nations Environment Programme, Global Environment Outlook 3. Earthscan Publications, Ltd., Sterling, VA. 2002. Earthscan Publications Ltd London • Sterling, VA, i-xxx1, 1-427 (2002).
37. Falcon-Rodriguez, C.I., Osornio-Vargas, A.R., Sada-Ovalle, I. & Segura-Medina, P. Aeroparticles, Composition, and Lung Diseases. Front Immunol 7, 3 (2016).
38. Li, D.Q., Chen, Z., Song, X.J., Luo, L. & Pflugfelder, S.C. Stimulation of matrix metalloproteinases by hyperosmolarity via a JNK pathway in human corneal epithelial cells. Invest Ophthalmol Vis Sci 45, 4302-4311 (2004).
39. De Paiva, C.S. et al. Corticosteroid and doxycycline suppress MMP-9 and inflammatory cytokine expression, MAPK activation in the corneal epithelium in experimental dry eye. Exp Eye Res 83, 526-535 (2006).
40. Novaes, P. et al. Ambient levels of air pollution induce goblet-cell hyperplasia in human conjunctival epithelium. Environ Health Perspect 115, 1753-1756 (2007).
41. Novaes, P. et al. The effects of chronic exposure to traffic derived air pollution on the ocular surface. Environ
Res 110, 372-374 (2010).
42. Gupta, S.K., Gupta, V., Joshi, S. & Tandon, R. Subclinically dry eyes in urban Delhi: an impact of air pollution? Ophthalmologica 216, 368-371 (2002).
43. Gupta, S.K. et al. A multicentric case-control study on the impact of air pollution on eyes in a metropolitan city of India. Indian J Occup Environ Med 11, 37-40 (2007).
44. Torricelli, A.A. et al. Effects of ambient levels of traffic-derived air pollution on the ocular surface: analysis of symptoms, conjunctival goblet cell count and mucin 5AC gene expression. Environ Res 131, 59-63 (2014).
45. Wiwatanadate, P. Acute air pollution-related symptoms among residents in Chiang Mai, Thailand. J Environ
Health 76, 76-84 (2014).
46. Lelieveld, J., Evans, J.S., Fnais, M., Giannadaki, D. & Pozzer, A. The contribution of outdoor air pollution sources to premature mortality on a global scale. Nature 525, 367-371 (2015).
47. Kim, K.H., Kabir, E. & Kabir, S. A review on the human health impact of airborne particulate matter.
Environment international 74, 136-143 (2015).
48. Global Burden of Disease Study, C. Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet 386, 743-800 (2015).
49. Baccarelli, A.A. et al. Particulate Air Pollution, Exceptional Aging, and Rates of Centenarians: A Nationwide
Analysis of the United States, 1980-2010. Environmental health perspectives (2016).
50. Martin, S., Dawidowski, L., Mandalunis, P., Cereceda-Balic, F. & Tasat, D.R. Characterization and biological effect of Buenos Aires urban air particles on mice lungs. Environ Res 105, 340-349 (2007).
51. Gomez, D.R., Fernanda Gine, M., Claudia Sanchez Bellato, A. & Smichowski, P. Antimony: a traffic-related element in the atmosphere of Buenos Aires, Argentina. Journal of environmental monitoring : JEM 7, 1162-1168 (2005).
52. Health effects of outdoor air pollution. Committee of the Environmental and Occupational Health Assembly of the American Thoracic Society. Am J Respir Crit Care Med 153, 3-50 (1996).
53. WHO’s global air-quality guidelines. Lancet 368, 1302 (2006).
54. Greepeace. Monitoreo de la Calidad del Aire de Buenos Aires. 2018:1-34.
55. Dockery, D.W. et al. Health effects of acid aerosols on North American children: respiratory symptoms.
Environmental health perspectives 104, 500-505 (1996).
56. Aires, A.d.P.A.G.C.A.d.B.
http://www.buenosaires.gob.ar/agenciaambiental/monitoreoambiental/laboratorio.
57. Li, D.Q. et al. JNK and ERK MAP kinases mediate induction of IL-1beta, TNF-alpha and IL-8 following hyperosmolar stress in human limbal epithelial cells. Experimental eye research 82, 588-596 (2006).
58. Cejka, C. & Cejkova, J. Oxidative stress to the cornea, changes in corneal optical properties, and advances in treatment of corneal oxidative injuries. Oxid Med Cell Longev 2015, 591530 (2015).
59. Tau, J. et al. Diesel exhaust particles selectively induce both proinflammatory cytokines and mucin production in cornea and conjunctiva human cell lines. Investigative ophthalmology & visual science 54, 4759-4765 (2013).
60. Hamrah, P., Liu, Y., Zhang, Q. & Dana, M.R. The corneal stroma is endowed with a significant number of resident dendritic cells. Investigative ophthalmology & visual science 44, 581-589 (2003).
61. Zheng, X., de Paiva, C.S., Li, D.Q., Farley, W.J. & Pflugfelder, S.C. Desiccating stress promotion of Th17 differentiation by ocular surface tissues through a dendritic cell-mediated pathway. Investigative ophthalmology & visual science 51, 3083-3091 (2010).
62. Stevenson, W., Chauhan, S.K. & Dana, R. Dry eye disease: an immune-mediated ocular surface disorder. Arch
Ophthalmol 130, 90-100 (2012).
63. Lasagni Vitar, R.M. et al. Evaluation of Oxidative Stress Markers in Human Conjunctival Epithelial Cells
Exposed to Diesel Exhaust Particles (DEP). Invest Ophthalmol Vis Sci 56, 7058-7066 (2015).
64. Tau, J. Efectos de la supeficie ocular sobre la superficie ocular: estudios in vitro. Doctor de la Universidad de
Buenos Aires, área Patología thesis, Universidad de Buenos Aires, 2017.
65. Gordon, S. & Taylor, P.R. Monocyte and macrophage heterogeneity. Nat Rev Immunol 5, 953-964 (2005).
66. Sica, A. & Mantovani, A. Macrophage plasticity and polarization: in vivo veritas. J Clin Invest 122, 787-795 (2012).
67. Galli, S.J., Borregaard, N. & Wynn, T.A. Phenotypic and functional plasticity of cells of innate immunity:
macrophages, mast cells and neutrophils. Nat Immunol 12, 1035-1044 (2011).
68. Hume, D.A. The Many Alternative Faces of Macrophage Activation. Front Immunol 6, 370 (2015).
69. Mosser, D.M. The many faces of macrophage activation. J Leukoc Biol 73, 209-212 (2003).
70. Mosser, D.M. & Edwards, J.P. Exploring the full spectrum of macrophage activation. Nat Rev Immunol 8,
958-969 (2008).
71. Briken, V. & Mosser, D.M. Editorial: switching on arginase in M2 macrophages. J Leukoc Biol 90, 839-841 (2011).
72. Overby, D.R. & Clark, A.F. Animal models of glucocorticoid-induced glaucoma. Exp Eye Res 141, 15-22 (2015).
73. Parisi, L. et al. Macrophage Polarization in Chronic Inflammatory Diseases: Killers or Builders? J Immunol
Res 2018, 8917804 (2018).
74. You, I.C. et al. Macrophage Phenotype in the Ocular Surface of Experimental Murine Dry Eye Disease. Arch
Immunol Ther Exp (Warsz) 63, 299-304 (2015).
75. Lee, H.S., Amouzegar, A. & Dana, R. Kinetics of Corneal Antigen Presenting Cells in Experimental Dry Eye
Disease. BMJ Open Ophthalmol 1, e000078 (2017).
76. Arora, S., Dev, K., Agarwal, B., Das, P. & Syed, M.A. Macrophages: Their role, activation and polarization in pulmonary diseases. Immunobiology 223, 383-396 (2018).
77. Colligris, B., Crooke, A., Huete-Toral, F. & Pintor, J. An update on dry eye disease molecular treatment:
advances in drug pipelines. Expert Opin Pharmacother 15, 1371-1390 (2014).
78. Kobayashi, A., Sugiyama, K., Li, W. & Tseng, S.C. In vivo laser confocal microscopy findings of cryopreserved and fresh human amniotic membrane. Ophthalmic Surg Lasers Imaging 39, 312-318 (2008).
79. Paolin, A. et al. Cytokine expression and ultrastructural alterations in fresh-frozen, freeze-dried and gamma- irradiated human amniotic membranes. Cell Tissue Bank 17, 399-406 (2016).
80. Hao, Y., Ma, D.H., Hwang, D.G., Kim, W.S. & Zhang, F. Identification of antiangiogenic and antiinflammatory proteins in human amniotic membrane. Cornea 19, 348-352 (2000).
81. Tseng, S.C., Li, D.Q. & Ma, X. Suppression of transforming growth factor-beta isoforms, TGF-beta receptor type II, and myofibroblast differentiation in cultured human corneal and limbal fibroblasts by amniotic membrane matrix. J Cell Physiol 179, 325-335 (1999).
82. Larson, B.J., Longaker, M.T. & Lorenz, H.P. Scarless fetal wound healing: a basic science review. Plast
Reconstr Surg 126, 1172-1180 (2010).
83. Rolfe, K.J. & Grobbelaar, A.O. A review of fetal scarless healing. ISRN Dermatol 2012, 698034 (2012).
84. Cowin, A.J., Holmes, T.M., Brosnan, P. & Ferguson, M.W. Expression of TGF-beta and its receptors in murine fetal and adult dermal wounds. Eur J Dermatol 11, 424-431 (2001).
85. Liechty, K.W., Adzick, N.S. & Crombleholme, T.M. Diminished interleukin 6 (IL-6) production during scarless human fetal wound repair. Cytokine 12, 671-676 (2000).
86. Liechty, K.W., Crombleholme, T.M., Cass, D.L., Martin, B. & Adzick, N.S. Diminished interleukin-8 (IL-8)
production in the fetal wound healing response. J Surg Res 77, 80-84 (1998).
87. Li, W., He, H., Kawakita, T., Espana, E.M. & Tseng, S.C. Amniotic membrane induces apoptosis of interferon-gamma activated macrophages in vitro. Exp Eye Res 82, 282-292 (2006).
88. He, H. et al. Suppression of activation and induction of apoptosis in RAW264.7 cells by amniotic membrane extract. Invest Ophthalmol Vis Sci 49, 4468-4475 (2008).
89. Hadis, U. et al. Intestinal tolerance requires gut homing and expansion of FoxP3+ regulatory T cells in the lamina propria. Immunity 34, 237-246 (2011).
90. Kordic, R. et al. Application of the amniotic membrane extract (AMX) for the persistent epithelial defect
(PED) of the cornea. Coll Antropol 37 Suppl 1, 161-164 (2013).
91. Dudok, D.V. et al. Effects of amniotic membrane extract on primary human corneal epithelial and limbal cells.
Clin Experiment Ophthalmol 43, 443-448 (2015).
92. Yam, G.H. et al. Ex Vivo Propagation of Human Corneal Stromal “Activated Keratocytes” for Tissue
Engineering. Cell Transplant 24, 1845-1861 (2015).
93. Tan, Y. et al. Amniotic membrane inhibits squamous metaplasia of human conjunctival epithelium. Am J Physiol Cell Physiol 301, C115-125 (2011).
94. Lee, S.B., Li, D.Q., Tan, D.T., Meller, D.C. & Tseng, S.C. Suppression of TGF-beta signaling in both normal conjunctival fibroblasts and pterygial body fibroblasts by amniotic membrane. Curr Eye Res 20, 325-334 (2000).
95. Kim, J.C. & Tseng, S.C. The effects on inhibition of corneal neovascularization after human amniotic membrane transplantation in severely damaged rabbit corneas. Korean J Ophthalmol 9, 32-46 (1995).
96. Tsubota, K. et al. Treatment of severe ocular-surface disorders with corneal epithelial stem-cell transplantation. N Engl J Med 340, 1697-1703 (1999).
97. Tsai, R.J., Li, L. & Chen, J. Reconstruction of damaged corneas by transplantation of autologous limbal epithelial cells(1). Am J Ophthalmol 130, 543 (2000).
98. Tsai, R.J., Li, L.M. & Chen, J.K. Reconstruction of damaged corneas by transplantation of autologous limbal epithelial cells. N Engl J Med 343, 86-93 (2000).
99. He, H., Zhang, S., Tighe, S., Son, J. & Tseng, S.C. Immobilized heavy chain-hyaluronic acid polarizes lipopolysaccharide-activated macrophages toward M2 phenotype. J Biol Chem 288, 25792-25803 (2013).
100. Lim, S.S. et al. A comparative risk assessment of burden of disease and injury attributable to 67 risk factors
and risk factor clusters in 21 regions, 1990-2010: a systematic analysis for the Global Burden of Disease Study
2010. Lancet 380, 2224-2260 (2012).
101. Shay, E., Khadem, J.J. & Tseng, S.C. Efficacy and limitation of sutureless amniotic membrane transplantation for acute toxic epidermal necrolysis. Cornea 29, 359-361 (2010).
102. Magatti, M. et al. Human amnion favours tissue repair by inducing the M1-to-M2 switch and enhancing M2 macrophage features. J Tissue Eng Regen Med 11, 2895-2911 (2017).
