ARCH ARGENT OFTALMOL | 2019
TRABAJO LIBRE
Rol de la salida uveoescleral en pacientes con hipotonía persistente post trabeculectomía (Estudio de la esclera con OCT-as)
Autores:
Dres. Gustavo Reca1, 2, Cecilia López1, Diego Pulfer1, Pablo Waimberg1, Julio Braillard1, Álvaro Fernández Mendy2, Lourdes Racca3
1 Swiss Medical, Bs. As., Argentina 2 Instituto de la Visión, Bs. As., Argentina 3Hospital Aeronáutico, Bs. As., Argentina
Contacto: recagustavo923@gmail.com
Recibido: 6/3/2019
Aceptado: 13/5/2019
Disponible en www.sao.org.ar
Arch. Argent. Oftalmol. 2019; 13: 45-52
RESUMEN
Objetivos: Estudiar la esclera, la conjuntiva y el cuerpo ciliar en pacientes con hipotonía post trabeculectomía resistente a tratamientos convencionales que intenten aumentar la presión ocular.
Métodos: Se estudiaron retrospectivamente 27 pacientes con diagnóstico de glaucoma primario de ángulo abierto, operados de trabeculectomía divididos en 3 grupos. Grupo 1: 4 pacientes con PIO media de 2 ± 1 mmHg con agudeza visual mejor corregida (AVMC) menor de 0.25. Grupo 2: 11 pacientes con PIO media de 8 ± 2 mmHg AVMC mayor de 0.6. Grupo 3: 12 pacientes con PIO mayor de 16 mmHg y AVMC mayor 0.65. Se agregó un Grupo 4 con 10 pacientes control, con PIO normales, sin cirugías previas ni medicación tópica ni sistémicas.
Criterios de exclusión: pacientes con colagenopatías, uveítis, escleritis, miopes, usuarios de corticoides tópicos o sistémicos.
Evaluaciones preoperatorias: agudeza visual corregida, biomicroscopía del segmento anterior y posterior, espesor de la capa de fibras de la papila y características de la esclera por OCT, campo visual computado, se descartaron causas de hipotonía: desprendimiento cilio-coroideo persistente y Seidel por Biomicroscopía anterior y posterior, biomicroscopía ultrasónica, y ecografía modo B. A todos los pacientes del Grupo 1 se les colocó dentro de los 60 días del postoperatorio lente de contacto de 16 mm, sangre autóloga y suturas de compresión de la ampolla, para intentar revertir la hipotonía. Posteriormente se realizó plástica de la ampolla y colocación de parche escleral, sin conseguir aumentar la PIO. Sólo estos 4 casos, revirtieron con vitrectomía y C3F8 o SF6.
Resultados: No hubo diferencia estadísticamente significativa en cuanto a la distribución de edad y sexo, para ninguno de los 4 grupos. La agudeza visual en los grupos 1 y 2 presentó una diferencia estadísticamente significativa (p < 0,001). AV: 0.3 ± 0.1 versus 0.6 ± 0.1. Entre los grupos 2, 3 y 4 no hubo diferencia significativa con respecto a la AV. La PIO fue estadísticamente menor en el grupo 1 (p < 0,001) y para el grupo 2 (p < 0,04), con respecto a los grupos 3 y 4. Grupo 1: 2 ± 1 mmHg, grupo 2: 8 ± 2 mmHg, grupo 3: 16 ± 4,5 mmHg y grupo 4: 16 ± 2,4 mmHg. La medicación utilizada fue en primer lugar, en todos los pacientes, fueron las prostaglandinas, en segundo lugar: la combinación de beta-bloqueantes, inhibidores de la anhidrasa carbónica, alfa-agonistas y/o sus combinaciones. En cuanto al daño glaucomatoso avanzado MD > 12 db en todos los grupos con glaucoma excepto los normales. En cuanto a las imágenes esclerales del OCT anterior en los grupos 1 y 2 se observaron áreas hiporreflectivas asociadas a desorganización de las laminillas esclerales, en comparación con áreas de reflectividad escleral normal (p < 0,001) en los grupos 3 y 4.
Conclusión: No existen reportes en la literatura que asocien estas alteraciones esclerales con un posible aumento de salida del humor acuoso por la vía úveoescleral post trabeculectomía, y menos que sea un mecanismo más por el cual la trabeculectomía reduce la presión ocular y otras cirugías de glaucoma. Estas alteraciones halladas a nivel de la esclera nos brindan la posibilidad de considerar que, además de la función filtrante de la ampolla, podría existir un aumento de la salida uveoescleral no convencional. Este aumento de la salida uveoescleral podría ser parte de la razón por la cual la hipotonía en estos casos sería difícil de revertir, favorecida por las alteraciones esclerales.
Palabras claves: hipotonía ocular, glaucoma, uveoescleral, trabeculectomía.
SUMMARY
Objectives: To study the sclera, conjunctiva and ciliary body in patients with post-trabeculectomy hypotony resistant to conventional treatments that attempt to increase the intraoocular pressure (IOP).
Methods: We studied retrospectively 27 patients with diagnosis of primary open angle Glaucoma, operated on with trabeculectomy divided into 3 groups. Group 1: 4 patients with a mean IOP of 2 ± 1 mmHg with best corrected visual acuity (BCVA) less than 0.25. Group 2: 11 patients with mean IOP of 8 ± 2 mmHg and BCVA greater than 0.6. Group 3:12 patients with IOP greater than 16 mmHg and BCVA more than 0.65. Group 4: 10 patients, with normal IOP, without previous surgeries or topical or systemic medication. Exclusion criteria: Patients with Connective tissue diseases, uveitis, scleritis, myopic, without topical or systemic corticoid. Preoperative evaluations: Corrected visual acuity, biomicroscopy of the anterior and posterior segment, thickness of the layer of fibers of the papilla and characteristics of the sclera by OCT, computed visual field, causes of Hypotonia were ruled out: detachment Cilia-persistent choroidal and Seidel by anterior and posterior biomicroscopy, ultrasonic biomicroscopy (UBM), and B-mode ultrasound. All patients in group 1 used a 16 mm contact lens within 60 days of the post-operative, autologous blood and compression sutures of the bleb, a bleb plastia with scleral patch trying to reverse the hypotonia, without success. Only these 4 cases reverted hypotony performing vitrectomy with inyection of C3F8 or SF6.
Results: There was no statistically significant difference in age and sex distribution for any of the 4 groups. Visual acuity comparing between Groups 1 and 2 showed a statistically significant difference (p < 0.001). AV: 0.3 ± 0.1 versus 0.6 ± 0.1. Considering BCVA between groups 2, 3 and 4 there was no significant difference. The IOP was statistically lower in Group 1 (p < 0.001) and Group 2 (p < 0.04), comparing to groups 3 and 4. Group 1: 2 ± 1 mmHg, group 2: 8 ± 2 mmHg, group 3: 16 ± 4.5 mmHg and group 4:16 ± 2.4 mmHg. Prostaglandins were the medication most used in all patients, the combination of beta-blockers, carbonic anhydrase inhibitors, alpha-agonists and/or their combinations were the second for advanced Glaucoma damage MD > 12 db in all groups 1 to 3. The scleral images of the OCT in Groups 1 and 2, showed hypo reflective areas associated with disorganization of scleral lamellae compared with normal scleral reflectivity (p < 0.001) in Groups 3 and 4.
Conclusion: So far there have been no reports associating these scleral changes with a possible increase of out flow of aqueous humor through the uveoscleral pathway among post-trabeculectomy patients. Neither that this could be a mechanism to reduce the IOP after glaucoma surgeries. These anatomical findings at the sclera let us consider the possibility that, in addition to the filtering function of the bleb, there could be an increase in the unconventional uveoescleral outflow. This increase in uveoscleral outflow would be part of the reason why hypotonia in these cases, favored by scleral alterations, could have been difficult to reverse.
Keywords: Ocular hypotony, glaucoma, uveoscleral, trabeculectomy.
INTRODUCCIÓN
El motivo de este trabajo es realizar el estudio de la esclera, la conjuntiva y el cuerpo ciliar en pacientes con hipotonía post trabeculectomía resistente luego de todos los tratamientos convencionales que intenten aumentar la presión ocular en estos casos.
Antes de hablar de los resultados sobre la evaluación de la esclera post trabeculectomía, es importante señalar que el aumento de la edad aumenta la rigidez de la esclera, alterándose las propiedades viscoelásticas, como su permeabilidad y su estructura molecular de la misma 23, 28, 29. La cirugía por excelencia del glaucoma sigue siendo aún la trabeculectomía especialmente en pacientes con daño avanzado y presión no controlada con máxima medicación médica y/o láser 1, 2, 3. En glaucoma leve y moderado disminuyó su indicación por tratamientos quirúrgicos mínimamente invasivos (MIGS)8,18,20,21,24,25,26,31,32 de rápida recuperación. En pacientes con alta tasa de posibilidad de fracaso de la trabeculectomía la indicación es la colocación de implantes de drenaje valvulados o no. 29, 30. Los pacientes operados de trabeculectomía pueden desarrollar ampollas filtrantes paredes finas, extensas, exuberantes, que controlan mejor la presión ocular, pero con más posibilidad de complicaciones, a veces severas disminuyendo la visión, aunque la principal vía de salida es el espacio subconjuntival y también se genera salida uveoescleral 4-8, 10, 11, 16. La trabeculectomía disminuye la PIO creando una fístula entre la cámara anterior y el espacio subconjuntival. Pero los nuevos dispositivos lo hacen aumentado la salida uveoescleral en general18, 22, 24, 25, 29, 31, 32, pero no existen reportes que la trabeculectomía baja también la PIO, aumentado la salida uveoescleral, y podría explicar porqué son refractarias, a diversos tratamientos propuestos para aumentar la PIO en algunos pacientes, dado que los tratamientos actúan sobre la ampolla filtrante 11, 12.
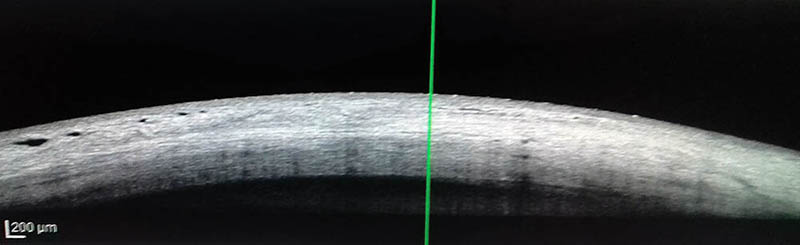
Figura 1: Esclera normal que presenta 3 áreas diferentes de reflectividad y observación de vasos colectores.
MATERIAL Y MÉTODOS
Se dividieron las pacientes en 4 grupos. Grupo 1: 4 pacientes con PIO media de 2 ± 1 mmHg y baja visión. Grupo 2: 11 pacientes con PIO media de 8 ± 2 mmHg y buena agudeza visual. Grupo 3: 12 pacientes con PIO > de 16 mmHg. Grupo 4: 10 pacientes control normales, sin cirugías, y o medicaciones que alteren la esclera: tópicas o sistémicas. Los grupos 1 al 3 fueron operados de glaucoma, con una trabeculectomía primaria con 5-FU intraoperatorio (50 mg/ml durante 5 minutos). Todos los pacientes (grupos 1 a 3) presentaban un solo diagnóstico clínico: glaucoma primario de ángulo abierto.
Criterios de exclusión: enfermedades sistémicas (especialmente colagenopatías), uveítis (en especial, escleritis), miopes22, 24, 25, usuarios de corticoides tópicos o sistémicos20.
Evaluaciones preoperatorias: agudeza visual, biomicroscopía del segmento anterior y posterior, espesor de la capa de fibras de la papila (OCT Spectralis), características de la esclera normal y pacientes, con hipotonía persistente, con OCT Spectralis). La esclera normal se caracteriza por poseer tres capas de diferente reflectividad por atenuación del paso de la luz láser y las áreas hiporreflectivas con sombras corresponden a vasos conjuntivales y epiesclerales y esclerales profundos y medios, que suelen dar sombras reflectivas, no así los intraesclerales superficiales o profundos. Mastropascua 23 considera áreas hiporreflectivas aquellas que son menores del 50% del promedio de intensidad de reflectividad de las tres capas normales o que estén alrededor con patrón normal. El campo visual computado (Octopus G1X TOP - progresión y estadificación del daño glaucomatoso). Se descartaron causas de hipotonía: desprendimiento cilio-coroideo persistente y Seidel+ (biomicroscopía anterior y posterior, UBM, ECO B). A todos los pacientes con hipotonía persistente con presiones de 2 ± 1 mmHg, que recibieron tratamiento y seguimiento durante 13 +- 7 meses, rango: de 3 a 52 meses se les colocó tempranamente, en algunos pacientes, (60 días postoperatorio), lente de contacto de 16 mm, sangre autóloga y suturas de compresión de la ampolla (Palmberg). Posteriormente se realizó plástica de la ampolla y colocación de parche escleral, tampoco hallando resultados positivos, aumentando la PIO. Por último vitrectomía con C3F8 o SF6.
ANÁLISIS ESTADÍSTICO
El t test Student, con el objetivo de evaluar diferencias de edad, PIO, sexo y daño glaucomatoso entre los diferentes grupos y χ2 para variables categóricas. Se utilizó ANOVA de una vía y correlación de Spearman para evaluar cambios estructurales significativos en la esclera entre los diferentes grupos, durante el seguimiento y el grado de correlación (fuerza y sentido) con la PIO, para una p < de 0,05. Dentro de los cambios esclerales se evaluó como cambio, zonas hiporreflectivas y de desorganización de las lamelas esclerales presente o no.
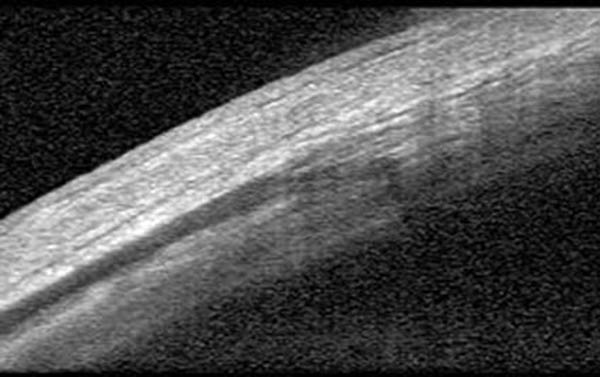
Figura 2: Esclera normal y músculo recto externo normal.
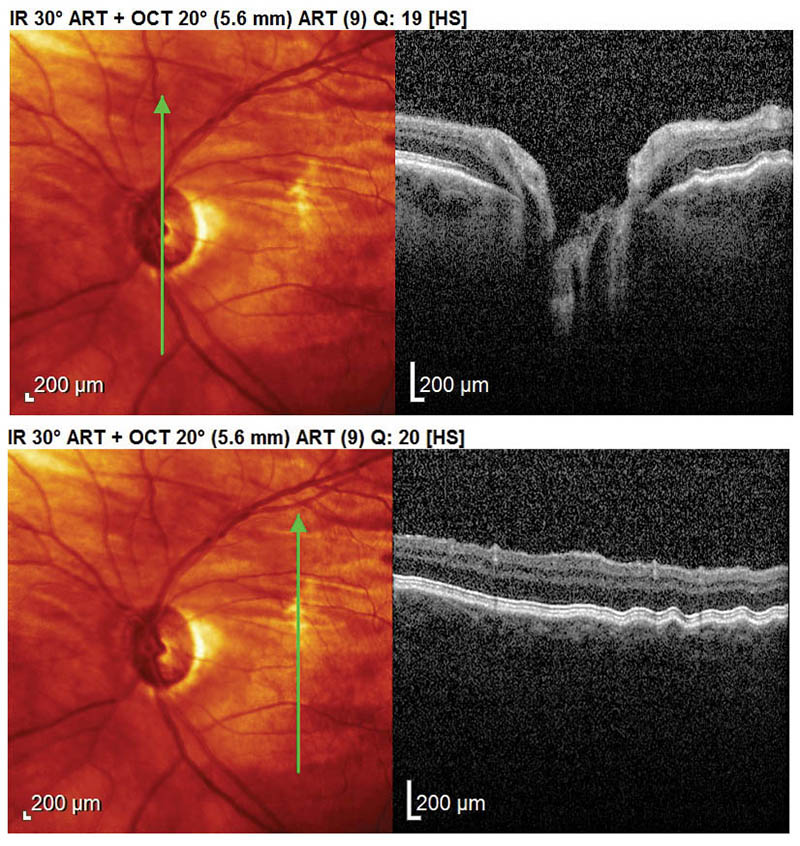
Figura 3: A) Hipotonía edema de papila. B) Pliegues retinocoroideos. Maculopatía hipotónica.
RESULTADOS
En cuanto a la edad y sexo no hubo diferencia estadísticamente significativa. En cuanto al grupo 1 (58 ± 21 años) hubo una tendencia a ser menor con respecto al valor medio del resto de los grupos de (65 ± 22 años), pero dado el bajo número de pacientes no se pudo aseverar estadísticamente. La escleras de los adultos jóvenes, no poseen alteraciones de rigidez, afinamiento, uniones de colágeno no alteradas y conservan en su primera capa de la esclera externa de elastina. Aun así, no explica porqué existiría una tendencia no significativa a la hipotonía, sin ampollas subconjuntivales filtrantes La agudeza visual en los grupos 1 y 2 presentaron una diferencia estadísticamente significativa (p < 0,001). AV: 0,3 ± 0,1 versus 0,6 ± 0,1. Entre los grupos 2, 3 y 4 no hubo diferencia significativa con respecto a la AV. En el grupo 2 no esperábamos hallar alteraciones escleras semejantes al grupo 1. La PIO fue estadísticamente menor en el grupo 1 (p < 0,001) y para el grupo 2 (p < 0,04), con respectos a los grupos 3 y 4. Grupo 1: 2 ± 1 mmHg, grupo 2: 8 ± 2 mmHg. grupo 3: 16 ± 4,5 mmHg y grupo 4: 16 ± 2,4 mmHg. La medicación utilizada fue en primer lugar las prostaglandinas, en segundo lugar, se adicionó: la combinación de beta-bloqueantes, inhibidores de la anhidrasa carbónica, alfa-agonistas y/o sus combinaciones en los pacientes con glaucoma avanzado, requieran más de una gota. Una vez que se operaron se suspendió toda medicación antiglaucomatosa. En el grupo 3, no se hallaron alteraciones esclerales aun recibiendo la misma medicación que los grupos 1,2. En cuanto al daño fue avanzado MD > 12db (criterio de Hoddap), el corte de 12 db se confirmándolo con estrategia umbral en más de tres oportunidades como la progresión del mismo 36. Oct de espesor de capa de fibras 58-+ 8 um, en el momento previo que se operaran y cuando progresaron se utilizó el cvc y oct en más de tres veces, para confirmarlo. En cuanto a las imágenes de OCT anterior en los grupos 1 y 2 se observaron áreas hiporreflectivas asociadas a desorganización de las laminillas esclerales, (p < 0,001) con respecto a grupos 3 y 4. En cuanto a la edad y sexo no hubo diferencia estadísticamente significativa. Se estudiaron los mismos grupos con UBM SONOMED, 35 MHZ con el fin de descartar desprendimiento cilio coroideo y ciclo-diálisis, en este estudio. Este estudio permite visualizar cuerpo ciliar y coroides y evalúa con poca sensibilidad la esclera.
DISCUSIÓN
No existen reportes que asocien estas alteraciones esclerales con la trabeculectomía y puedan relacionarse con un posible aumento de salida del humor acuoso por la vía uveoescleral post trabeculectomía, y menos que sea un mecanismo por el cual la trabeculectomía reduce la presión ocular. La trabeculectomía disminuye la presión ocular al crear una fístula que comunica la cámara anterior y el espacio subconjuntival permitiendo de esta manera el drenaje del humor acuoso, inicialmente descripta por Cairns1 en 1968, Watson y Barnett2 en 1975 y fue considerada el Gold Standard de la cirugía de glaucoma, siendo aún hoy la primera elección en pacientes con presiones elevadas que no regulan con medicación y/o laser en pacientes con daño avanzado (>12db y progresivo el CVC es muy fluctuantes más cuando es avanzado por eso es importante realizar más tres campos visuales que disminuye a cambios de 4 a 2, 0,5 Db/Año, db 80%) 36. En cuanto al oct espesor de capa de fibras con cambios mayores de 3um sería posible afirmar progresión, a pesar del poco tejido a evaluar. La trabeculectomía en la mayoría de los casos, fracasa por la excesiva cicatrización del espacio subconjuntival 1-3. La modificación de la cicatrización previniendo una proliferación excesiva de los fibroblastos con el uso de antimetabolitos, permite alcanzar una tasa de éxito, pero disminuyendo su seguridad 4, 7, 8, 9, 10, 13. Los antimetabolitos, en especial la Mitomicina, son cien veces más potentes que el 5-FU y se asocian a una mayor tasa de éxito y de complicaciones como el Seidel+, temprano o tardío, ampollas extensas exuberantes de paredes finas que favorecen la hipotonía ocular 11, 12, 13, 16, blebitis y endoftalmitis, afinamiento de la esclera, causas importantes de disminución de la visión 3, 9, 10, 11. Se define hipotensión ocular10, 11, 12 a pacientes con presiones menores de 5 mmHg, con disminución de visión, edema de papila y pliegues retino-coroideos, maculopatía hipotónica descripta por Dellaporta, en 195511 y Gass12. Los antimetabolitos suelen ser la principal causa de hipotonías post quirúrgicas 7, 8, 12, pero existen otros factores como la rigidez escleral que puede ser modificada por la miopía, edad y prostaglandinas2, 15-17, 19, 20, 23, 24. Existe un parámetro por sistema ORA que mide la histéresis corneal, que es un índice de elasticidad ocular que nos permite medir con bastante sensibilidad y especificidad la disminución de la rigidez escleral, a medida de que aumenta la edad, incluso más exacto que el espesor corneal28, 29. La edad aumenta la rigidez escleral 29, puede oscilar su espesor de 400 a 1000 µm, compuesta esencialmente por una matriz extracelular, sintetizada por grupos celulares de colágeno, alterándose preferentemente la esclera con la edad a nivel limbal como peripapilar. Con el aumento de la edad se alteran las propiedades biomecánicas volviéndose más rígida, fina, pero con uniones celulares que se vuelven más débiles. Por otro lado, no todos los sectores de la esclera (anisotropía), poseen las mismas propiedades viscoelásticas29. Todos los pacientes recibieron prostaglandinas 23 que alteran la matriz extracelular y 5-fluoruracilo 17 que también pueden alterar el colágeno. Estas alteraciones nos generan nuevas líneas de investigaciones, pero con escaso número de pacientes es imposible afirmar o negar que las prostaglandina o el 5 fluoruracilo influyó en los resultados. También observamos esta alteración escleral en pacientes con hipotonía relativa, con presiones de 8 ± 2 mmHg con buena agudeza visual. Se describe también la hipotonía y disminución de la PIO en la cirugía no penetrante sin ampollas filtrantes, en aquellos pacientes con presiones bajas y sin ampolla filtrante, y como mecanismo de disminución exitosa en pacientes post-ciclo-fotocoagulación con diodo láser por pulsos y crioterapia 14, 17-18 y dispositivos de drenaje coroideo 23, válvulas a los 6 meses o cuando tenemos ampollas avasculares, observación personal. Algunos autores describieron el patrón multicapa y zonas no reflectivas esclerales, en una ampolla hiperfiltrante con Seidel positivo, pero no hacen referencia o correlación a la disminución de PIO por aumento de la salida uveoescleral 16, 23. No hay trabajos con grupo control glaucomatoso con el mismo diagnóstico y cirugía primaria con presiones > de 16 mmHg con ampollas con fibrosis con o sin medicación tópica y normales, no miópicos14, 24, sin cirugías y/o medicación tópica o sistémicas. Sin duda nuestra afirmación es indirecta por los hallazgos en la esclera y asociación con la clínica, los datos. El flujo uveoescleral se puede estimar con trazas radioactivas o fluorometría18, 19. En los dispositivos de drenaje coroideo aumentan la salida uveoesclerales estudiando también un estudio de estos casos se observó aumento de imágenes hiporreflectivas también por debajo del nivel del cuerpo ciliar y coroideo rodeando al dispositivo en la esclera pero el drenaje es esencialmente a través de los vasos venosos cilio-coroideos21-25. Se ha observado un mayor número áreas hiporreflectivas por debajo de los músculos, posiblemente la esclera es más fina en los lugares de inserción. También el aumento de áreas hiporeflectivas al bajar la PIO, aumente el flujo de los vasos esclerales y epi-esclerales. Estas mismas imágenes hiporreflectivas se observan post crioterapia y ciclo-fotocoagulación con diodo láser14, 15. El tallado de tapas esclerales gruesas, profundas, y cerradas herméticamente podría aumentar la salida uveoescleral. El significado clínico y fisiología del rol de salida del humor acuoso por la vía convencional es difícil de medir en seres humanos in vivo 18, 19. De acuerdo al animal estudiado el porcentaje de salida puede variar de un 3%, 15% y 60%26. Toris22 y colaboradores estudiaron la dinámica del flujo uveoescleral en hipertensos oculares y fue mucho menor que en normales y en pacientes con glaucoma avanzado que no controlaban la PIO con máxima medicación tolerable, a pesar de que la PIO sólo influye en la salida uveoescleral en valores muy extremos menores de 4 mmHg o mayores de 60 mmHg. El aumento de salida trabecular es lineal con respecto al aumento de PIO en cámara anterior, lo mismo ocurre cuando se realiza la trabeculectomía, que genera un gradiente de presión que existe entre la cámara anterior y el espacio subconjuntival sin fibrosis excesiva.
Volviendo a la salida no convencional, los músculos ciliares son la principal barrera al pasaje de humor acuoso, no hay barrera epitelial y el gran flujo se hace hacia los vasos ciliocoroideo y un porcentaje menor a través de la esclera (conductibilidad de la esclera: 4.3 µL/min – Jackson et al 2006), haciendo que el humor acuoso drene alrededor de los vasos esclerales que atraviesan la esclera o forman un plexo hacia los vasos ciliocoroideo. La ciclo-diálisis, separación del cuerpo ciliar de la esclera, se puede aumentar hasta un 50% la salida uveoescleral bajando la PIO y la compresión del cuerpo ciliar la disminuye indicando, que el cuerpo ciliar constituye también la principal resistencia a la vía no convencional 22.
Ambas vías disminuyen por el aumento de la presión venosa epiescleral, pero en menor medida en la vía no convencional. Lo mismo ocurre con la PIO de la cámara anterior 22. Existen diversos reportes11, 12, 16 que incluyen tratamientos para subir la PIO en ojos con hipotonía persistente en ojos con trabeculectomía primaria con Mitomicina C: lentes de contacto de 16 mm, inyección de sangre autóloga, facoemulsificación, resutura, colgajo escleral, colocación de parche escleral, lente de Savage y Simmons, puntos de compresión de la ampolla (Palmberg), y vitrectomía con C3F8 o SF6 34, 35. Siendo esta última cirugía que revirtió estos ojos que no funcionaron con los métodos habituales. El objetivo de este trabajo es describir la esclera con un OCT-as en pacientes con PIO de 2 ±1 mmHg y pérdida de visión y de 8 ± 2 mmHg con visión. Posiblemente la salida uveoescleral aumentada en estos pacientes y las imágenes que revirtieron, post-vitrectomía, C3F8 o SF6 34-35, no habiendo delaminación de esclera, pocas zonas hiporreflectivas como los pacientes on PIO > de 16 mmHg sin medicación en el momento del estudio escleral y normales no se halló ni delaminación y ni zonas hiporreflectivas esclerales. Posiblemente la salida de humor acuoso uveo-escleral esté aumentada en pacientes con zonas de desorganización de láminas esclerales y zonas de hiporreflectividad con hipotonía de 2 ± 1 mmHg con pérdida de visión e igualmente en paciente a 8 ± 2 mmHg con agudeza visual conservada. Quizás sea el mecanismo extra de filtración de humor acuoso porque ciertas hipotonías, difíciles de tratar, pueden revertirse con vitrectomía y C3F8 o SF6 34-35 comprimiendo la esclera y el cuerpo ciliar, drenando humor acuoso y al cicatrizarse con el tiempo desaparecen las zonas hiporreflectivas y delaminación en la esclera.
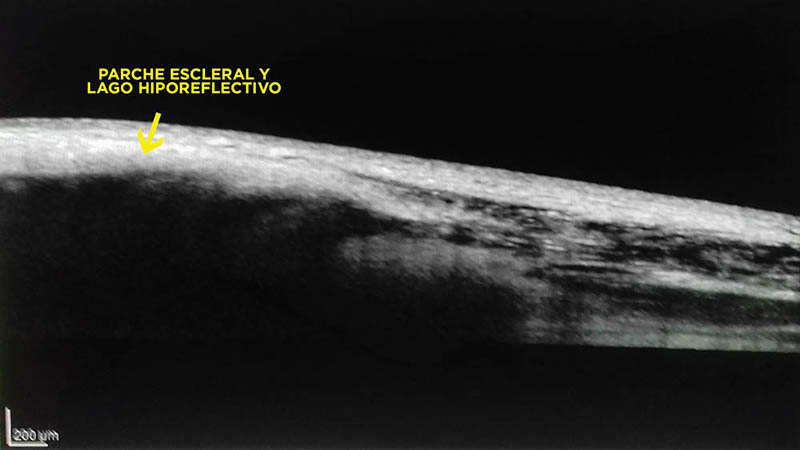
Figura 4: Observación de la esclera en pacientes con hipotonía persistente aún con parche escleral. La esclera presenta desorganización de las lamelas de fibras de colágeno y áreas hiporreflectivas.
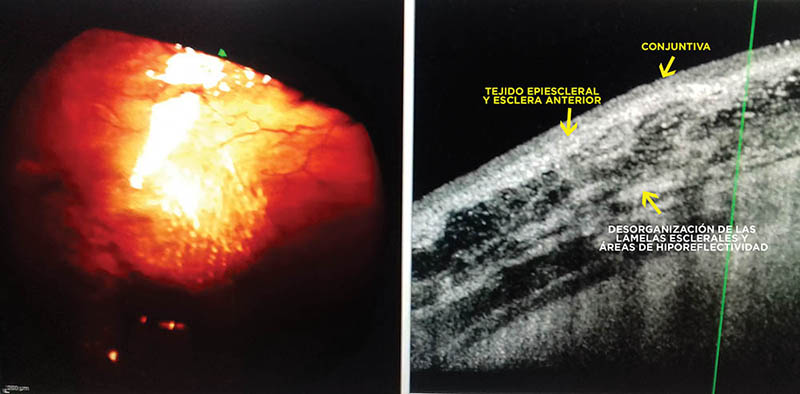
Figura 5: Magnificación de la imagen de la figura 04.
CONCLUSIÓN
Estas alteraciones a nivel de la esclera nos brindan la posibilidad de considerar que, además de la función filtrante de la ampolla, existe un aumento de la salida uveoescleral no convencional, para disminuir la PIO. Esto podría generar una mayor dificultad al tratar cuando estos pacientes desarrollan hipotonía persistente a los métodos habituales para aumentar la PIO, además de explicar la razón por la cual estas cirugías sin ampollas tienen presiones bajas 19, 20 y otras cirugías son efectivas sin ampollas filtrantes, no penetrante, canaloplastia y dispositivos de drenaje coroideo.
Los autores de este artículo no tienen intereses comerciales en ningún material de los presentados en este artículo.
BIBLIOGRAFÍA
1. Cairns JE. Trabeculectomía, reporte preliminar de un nuevo método. Am Ophthalmol 1968 66:673-679.
2. Watson PG, Barnett F. Effectiveness of Trabeculectomy in Glaucoma. Am Ophthalmol. 1975:798 31-45.
3. Reza Razenghinejad M, Spaeth GL et al. Mayor Review The Changing Conceptual Basis of Trabeculectomy: A Review of Past and Current Surgical Technique. Surv Ophthalmol 57:1-25, 2012.
4. Wong FRCOphth TT el al. The Singapore 5-Fluorouracil Trabeculectomy Study. Effects on Intraocular Pressure Control and Disease Progression at 3 years. Ophthalmology 2009:116;175-184.
5. Palanca-Capristano AM, WuDunn D et al. Long-term Outcomes of introperative 5-Fluoruracil versus Mitomycin en Primary Trabeculectomy Surgery. Ophthalmology 2009:116;185-190.
6. Reca G, Cingolani C y col. 5 Fluorouracilo intraoperatorio en trabeculectomía inicial en el Glaucoma Primario de Ángulo Abierto. Archivos de Oftalmología 1995: Vol 70; 29-39.
7. Hu CY, Tanaka S et al. Clinical Characteristic and Leakage of Funtioning Blebs After Traculectomy with Mitomicyn-C In Primary Glaucoma Patients. Ophthalmology:2003: (1)10:345-352.
8. Bahler C, Hann C et al. Second-generation trabecular meshwork by pass stent (iSent inject) increases outflow facility in culture human anterior segments. Am J Ohthalmol. 2012:153;1206-13.
9. Stamper L, Lieberman MF et al. Hypotonus Maculopathy after Trabeculectomy With Subconjuntival 5-Fluouracil. Am J. Ophthalmol 1992 114:544-553.
10. Viviane RF, Ruthanne B, Pakter HM, Simmons RJ. Hipotonía persistente tras trabeculectomía primaria con Mitomicina C. Arq Brasieres Oftalmol. Vol 63 no.3 Sao Paulo, junio 2000.
11. Dellaporta A. Cambios de fondo en hipotonía postoperatoria. Am J. Ophthalmol 1955: 40:781-785.
12. Gass DM. Maculopatía Hipotónica. Bellow JG, Ed. Oftalmología contemporánea. Baltimore: William y Wilkins; 1972; 34.
13. Nuyts RMM, Greve EL et al. Treatment of Hypotonus Maculopathy, Trabeculectomy Mitomycin C. Am J Ophthalmol 1994;118:322-331.
14. Savage, J.A., Condon G.P. et al Lisis after trabeculectomy, Ophthalmology 1988; 95:1631-1637.
15. Guedes V.R.F., Ruthanne B. Simmons Hipotonía persistente tras trabeculectomía primaria con Mitomicina C., Arq. Brasieres Oftalmol. Vol 63 no.: 3 Sao Paulo junio 2000.
16. Shields MB et al. Clinical and Histophathologic observation concerning hypotony after with Mitomycin C. Am J. Ophthalmol. 1993; 116: 673-683
17. Olsen T, Edelhauser H, Lim J et al. Human Scleral Permeability, Effects of age, cryotherapy, trans scleral diode laser, and surgical thinning. Invest Ophthalmol Vis Sci. 1995; 36: 1893-1903-5.
18. Mastropasqua R, Agnifili L et al. Uveo-scleral outflow pathways after ultrasonic cyclocoagulation in refractory glaucoma: an anterior segment Optical Coherence Tomography and in vivo confocal Study. Br J Ophthalmol. 2016; 100:1668-1675.
19. Cerdá-Ibáñez M, Pérez-Torregrosa VT et al. Análisis cualitativo de ampollas de filtración reparadas mediante tomografías de coherencia óptica del segmento anterior. Archivos de la Sociedad Española de Oftalmología. 2017; 92(8):359-365.
20. Ito K, Matsunaga K et al. Supraciliocoroidal fluid in the ayes indicates good intraocular pressure control despite absence of obvious filtering bleb after Trabeculectomy. J Glaucoma. 2002 Dec; 11 (6): 540-542.
21. Bill A. Uveoscleral drainage of aqueous humor: physiology and pharmacology. Prog Clin Biol Res. 1989; 312: 417-427.
22. Toris CB, Yablonsky ME et al. Aqueous humor dynamics in the aging human eye. Am J Ophthalmol. 1999; 127 (4): 407- 412.
23. Lindsey JD, Kashiwagi K et al. Prostaglandins alter extracelular matrix adjacent to human ciliary muscle cells in vitro. Invest Ophthalmol Vis Sci. 1997; 38 (11): 2214-2223.
24. Alm A, Nilsson Siv FE. Uveoscleral outfow – A Review Experimental Eye Research, 88 (2009); 760-768.
25. Reca G, Fernández Mendy A at al. Evaluación, seguridad y eficacia del dispositivo del drenaje coroideo Star Flo para disminuir la presión ocular versus trabeculectomía con 5 Fluorouracilo intraoperatorio. Archivos Argentinos de Oftalmología. 2017; mayo (8): 64- 75.
26. Smit BA, Johnstone MA, Effects of viscoelastic injection into Schlemm canal in primate and human eyes: potencial relevance to viscocanalostomy. Ophthalmology 2002; 109:786-792.
27. Sanchez E, Schyndler CC et al. Deep sclerectomy: results with and without colagen implant. Int Ophthalmol 1996-1997;20: 157-162.
28. Aitor LI, Perez-Lopez M. Relationship in Corneal Hysteresis and lamina cribosa displacement after medical reduction of intraocular pressure Br J Ophthalmol 2017; 101: 290-294.
29. El Sayyad F, Helal M, Elsherif Z et al Molteno implant versus Trabeculectomy with adjuntive intraoperative mitomycin-C in high risk glaucoma patients. J Glaucoma 1995; 4:80-85.
30. Gedde SJ, Brandt JC et al Tube versus Trabeculectomy Study Group Study Design and baseline characteristic of Study patients. Am J Ophthalmol 2000;130;267-73.
31. Skaat A, Sagir O et al. Gold micro-shunt implants versus Ahmed Glaucoma Valve: long term outcomes of a prespective randomized Clinical Trial J. glaucoma 2016;25;155-161.
32. Shaaraway TM, Sherwood MS et al. Devices in development glaucoma y and new procedures” Glaucoma Medical Diagnosis & Therapy. Elsevier 2015.
33. Gedde S et al. Post-operative complications in the tubo vs Trabeculectomy (TVT) Study during 5 years of folow up”. Am. J. Ophthalmol 2012;153;804-14.
34. Strank V.M., Pencak M, et al. 25 Gauge Vitrectomy and gas for the management of rhegmatogemous retinal detachment J. Glaucoma 2015; december 24; 9: 679.
35. Jawward M., Khan B. et al, Abotabad 2015 Oct-Dec (4)798-805.
36. Wu S, Medeiros F.P. et al VF testing Frequency to detect Progression. Ophthalmology 2017; 124:786-792.